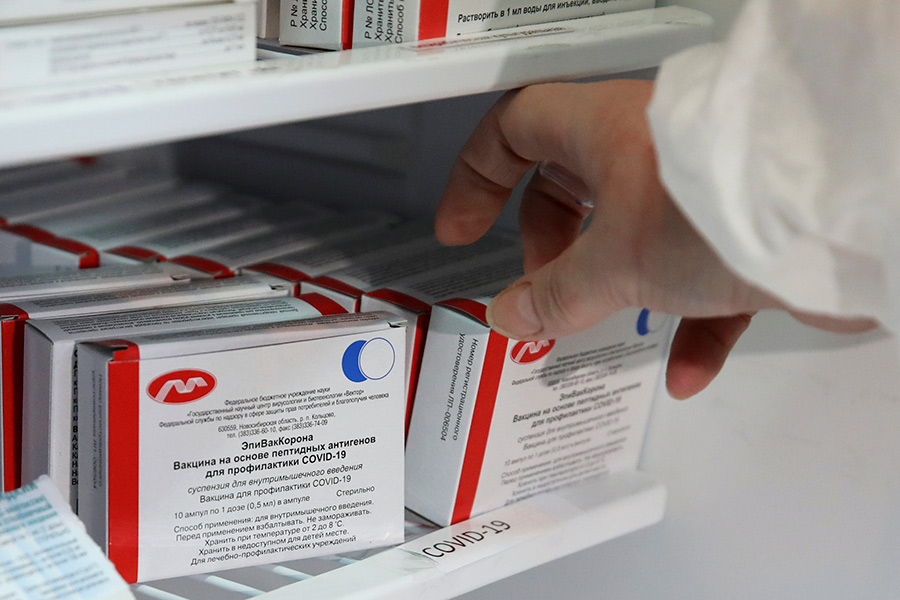
11 августа 2020 года Владимир Путин объявил о регистрации первой в мире вакцины против COVID-19 — российского препарата «Спутник V». Сегодня он зарегистрирован в 69 странах с общим населением более 3,7 млрд человек. По количеству полученных одобрений государственными регуляторами вакцина занимает второе место в мире. В Сан-Марино уже практически удалось достичь коллективного иммунитета благодаря «Спутнику V» и начал развиваться вакцинный туризм, рассказал «Известиям» министр здравоохранения и общественной безопасности республики Роберто Чаватта. Он поделился, что в страну приезжают специально, чтобы привиться российским препаратом.
Вечно первая
Россия первой в мире 11 августа 2020 года зарегистрировала вакцину от COVID-19, получившую название «Спутник V». Препарат разработан при поддержке Российского фонда прямых инвестиций (РФПИ) Национальным исследовательским центром эпидемиологии и микробиологии имени Н.Ф. Гамалеи.
Фото: ИЗВЕСТИЯ/Андрей Эрштрем
— Создание «Спутника V» — великое достижение Национального исследовательского центра эпидемиологии и микробиологии и отечественной науки в целом, — подчеркнул в беседе с «Известиями» руководитель лаборатории биологии и индикации арбовирусов Центра имени Н.Ф Гамалеи профессор Александр Бутенко. — По разным критериям это лучшая вакцина из всех существующих. Подтверждение — июльская публикация в международном журнале Vaccines. Авторы испытали возможности «Спутника V» против новых штаммов коронавируса. Оказалось, что антитела образуются против всех штаммов.
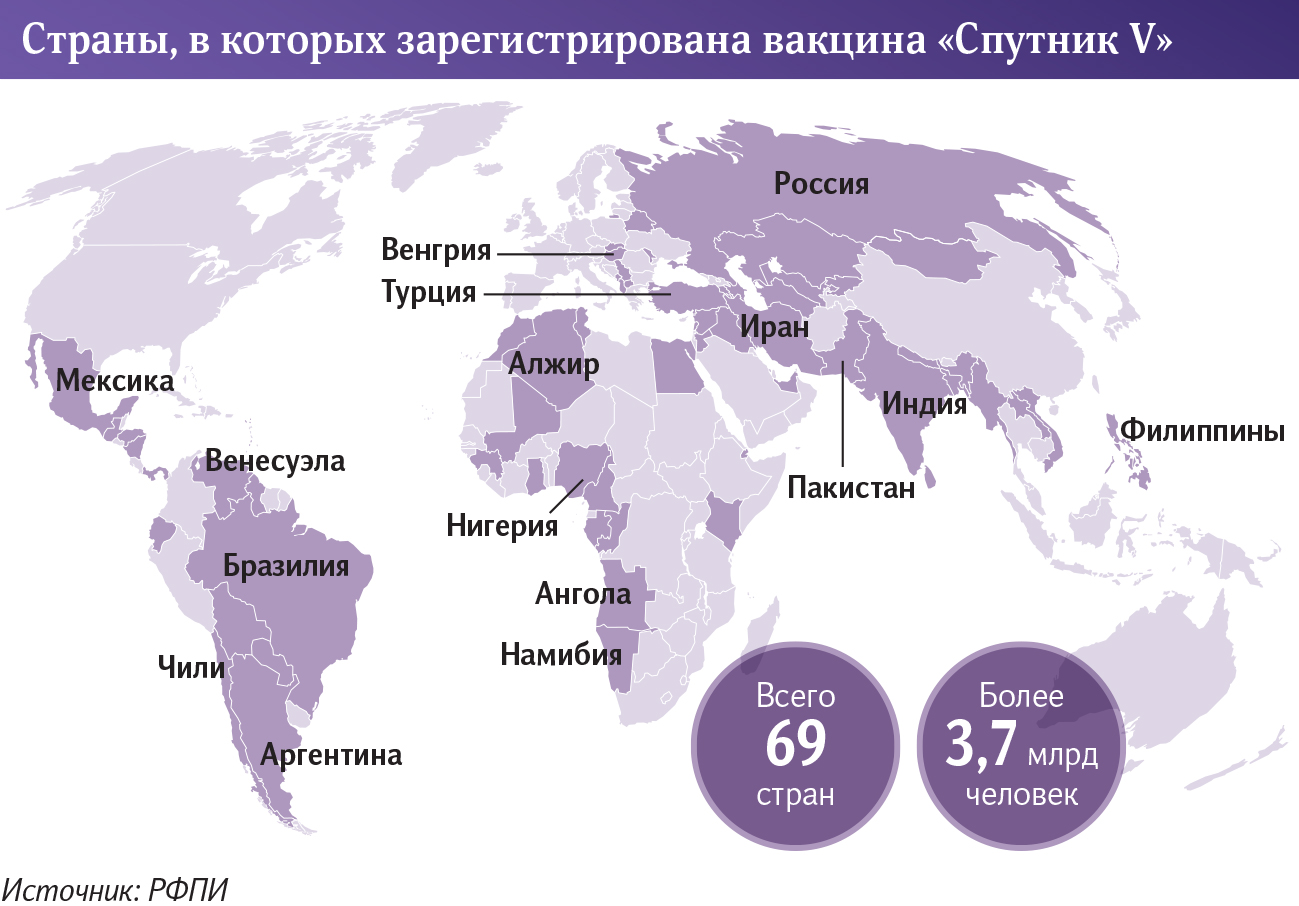
Сегодня «Спутник V» зарегистрирован в 69 странах с общим населением более 3,7 млрд человек. По количеству полученных одобрений государственными регуляторами вакцина занимает второе место в мире. Такие сведения «Известиям» предоставили в РФПИ. Данные от регуляторов стран, полученные в ходе вакцинации населения, доказывают, что «Спутник V» — одна из наиболее безопасных и эффективных вакцин против коронавируса, сообщает фонд на своем сайте.
Помимо России препарат производят в Узбекистане, Белоруссии, Аргентине, Вьетнаме. РФПИ объявил о партнерствах для производства вакцины с 20 компаниями в 14 государствах.
Вакцину разрабатывали в период, когда доминировал вариант вируса из Уханя. Спустя год оказалось, что она эффективна в том числе и против новых штаммов. Так, исследование, которое в июне провел минздрав аргентинской столицы, подтвердило высокую эффективность «Спутника V» против бразильского штамма коронавируса.
2 февраля 2021 года авторитетный научный журнал The Lancet опубликовал результаты третьей фазы клинических испытаний «Спутника V». Эффективность вакцины против заражения коронавирусом составила 91,6%.
Качество и количество
«Спутник V» создан на проверенной и хорошо изученной платформе аденовирусных векторов человека. Российская вакцина использует два разных вектора для двух прививок в ходе одного курса вакцинации. Такой метод обеспечивает более продолжительный иммунитет по сравнению с технологией одного и того же механизма доставки для обеих прививок.
По словам профессора Александра Бутенко, разработка вакцин такого типа — крайне перспективное направление на многие годы вперед.
«Спутник V» дал импульс развитию не только науки, но и фарминдустрии.
— С момента регистрации вакцины к ее производству подключилось семь производственных площадок, — сообщили «Известиям» в пресс-службе Минпромторга. — Они планомерно наращивают объемы производства, модернизируют свои производственные мощности для обеспечения потребности страны в вакцине, — добавили в ведомстве.
Фото: ИЗВЕСТИЯ/Павел Волков
Эксперты рынка дают ту же оценку.
— Удалось быстро организовать промышленный выпуск препарата, а затем масштабировать его производство сразу на нескольких площадках, — сказал «Известиям» директор по развитию компании RNC Pharma Николай Беспалов. — Начались поставки препарата на российский и зарубежные рынки, затем последовали публикации о результатах применения препарата, так сказать, в «боевых условиях». Наконец, за счет поставок «Спутника V» кратно вырос российский фармэкспорт.
Сегодня в нашей стране привиты 38,9 млн человек, заявил глава Минздрава Михаил Мурашко 5 августа на правительственном совещании. Подавляющее большинство россиян вакцинированы «Спутником V».
«Ни одного отрицательного отзыва»
В январе 2021 года РФПИ подал заявление на регистрацию препарата «Спутник V» в Европейском агентстве лекарственных средств (EMA). Пока что в Европе российскую вакцину зарегистрировали только отдельные страны, в частности Сан-Марино. По словам министра здравоохранения и общественной безопасности республики Роберто Чаватты, здесь предпочли привиться «Спутником», а не ждать, когда производители четырех одобренных в Европе вакцин решат проблемы с поставками. Больше того, в Сан-Марино ездят специально за российской прививкой.
— К нам приезжают люди со всего мира, — рассказал «Известиям» Роберто Чаватта. — В рамках вакцинного туризма мы сделали уже около 1,7 тыс. прививок. Всё идет отлично. В ближайшие недели мы продолжим вакцинацию, и так до сентября. По вакцине «Спутник V» мы не получили ни одного отрицательного отзыва. Это подтверждает ее эффективность. В стране уже практически удалось достичь коллективного иммунитета.
Фото: ИЗВЕСТИЯ/Дмитрий Коротаев
Чиновник рассказал об исследованиях российской вакцины, проведенных совместно с Болонским университетом и институтом «Спалланцани» в Риме.
— Нам подтвердили, что благодаря препарату в организме вырабатывается достаточно качественных антител, — добавил министр.
Еврокомиссия признает сертификаты о вакцинации, выдаваемые в Сан-Марино. Они теперь действительны на всей территории ЕС и в странах Шенгенской зоны. Однако с регистрацией «Спутника V» Европа не спешит.
— В Европе поддерживают свою фармпромышленность, и пускать чужаков на свой рынок им ни к чему, — предположил Николай Беспалов.
Российский фонд прямых инвестиций ожидает, что EMA одобрит российскую вакцину от коронавируса «Спутник V» осенью. Об этом в июле заявил глава РФПИ Кирилл Дмитриев.
В 2020 году силы ученых медиков и научных лабораторий по всему миру были брошены на разработку эффективных вакцин от Covid-19.
Сегодня по всему миру в процессе создания и тестирования находятся, по меньшей мере, 73 вакцины. 6 вакцин уже применяются в разных странах, а их разработчики стали настоящими героями в борьбе с общемировой угрозой.
Кто эти люди? Где учились создатели вакцин от Covid-19, и чем еще они занимаются?
Ниже расскажем об ученых, которые стоят за изобретением уже одобренных вакцин от коронавируса по всему миру…
Moderna
Самая известная американская вакцина от Covid-19 была разработана компанией Moderna, расположенной в городе Кембридж, штат Массачусетс. Это крупная биотехнологическая компания, сфокусированная на разработке лекарств и вакцин на основе технологий работы с матричной РНК. Само расположение компании способствует ее тесному сотрудничеству с учеными из ведущих американских университетов. Дело в том, что Кембридж (как и его британский тезка) известен как студенческий город и важный центр образования в США. Здесь находятся сразу два престижных американских вуза – Гарвардский университет и Массачусетский технологический институт.
Во главе разработки вакцины Moderna стоит Таль Закс, главный врач Moderna и бывший руководитель отдела глобальной онкологии в Sanofi. С 1986 по 1992 год Закс учился в Университете Бен-Гуриона в Негеве (Израиль), где получил степени M.D. и PhD.
После окончания вуза Таль Закс занимался научными исследованиями в U.S. National Institutes of Health, прошел клиническую практику в госпитале Университета Темпл (США) и стажировку в области медицинской онкологии в Пенсильванском университете (США).
Закс начал свою карьеру в GlaxoSmithKline, где занимался генетическими исследованиями. Сегодня он не только возглавляет компанию Moderna, но и является профессором медицины Пенсильванского университета. В 2020 году Таль Закс получил специальную награду за вклад в борьбу с коронавирусом от своей израильской альма-матер, Университета Бен-Гуриона.
BioNTech-Pfizer
Лидирующая европейская вакцина от Covid-19 была разработана в сотрудничестве немецкой биотехнологической компанией BioNTech и американским фармацевтическим гигантом Pfizer. Во главе компании BioNTech из немецкого города Майнц стоят ученые Угур Шахин и его жена Озлем Тюречи. Они не только представляют собой крепкий научно-исследовательский и семейный тандем, но и олицетворяют так называемую «европейскую мечту», ведь оба являются выходцами из семей трудовых мигрантов из Турции.
Угур Шахин известен как врач-иммунолог, специализирующийся на исследованиях рака. Он является основателем и генеральным директором биотехнологической компании BioNTech. Шахин переехал в Германию с семьей в возрасте 4 лет, вырос в Кельне и изучал медицину в Кельнском университете, где получил степень PhD в области иммунотерапии рака.
После окончания вуза Угур Шахин занимался научными исследованиями в госпиталях при Саарском университете (Германия) и Цюрихском университете (Швейцария), после чего основал собственную исследовательскую группу и стал профессором экспериментальной онкологии в медицинской клинике при Университете Майнца (Германия).
Не уступает Шахину и его супруга Озлем Тюречи — врач, ученый, предприниматель и соучредитель компании BioNTech. Будучи дочерью врача и биолога, Озлем изучала медицину в Саарском университете в и получила докторскую степень на медицинском факультете Саара в 1992 году. После этого она проходила хабилитацию и стажировку по специальной программе в German Research Foundation.
Исследования Озлем Тюречи сосредоточены на идентификации и характеристике опухолеспецифических молекул и разработке иммунотерапевтических средств для борьбы с раком. В 2002 году она завершила хабилитацию в Университете Йоханнеса Гутенберга в Майнце в области молекулярной медицины.
Oxford-AstraZeneca
Это еще одна европейская вакцина от Covid-19, разработанная совместно шведско-британским производителем лекарств и Оксфордским университетом. Со стороны Оксфордского университета над вакциной работала исследовательская группа, состоящая из 300 ученых, во главе с профессором Сарой Гилберт.
Сара Гилберт является британским вакцинологом, профессором вакцинологии в Оксфордском университете и сооснователем Vaccitech. Гилберт специализируется на разработке вакцин против гриппа и новых вирусных патогенов. Ранее она уже руководила разработкой и тестированием универсальной вакцины против гриппа, которая прошла клинические испытания в 2011 году. 30 декабря 2020 года вакцина от Covid-19, которую она разработала совместно с Oxford Vaccine Group, была одобрена для использования в Великобритании.
Как признается сама Гилберт, уже в детстве она поняла, что хочет посвятить свою жизнь медицине. После окончания школы Сара получила степень бакалавра биологических наук с отличием в Университете Восточной Англии (Великобритания), а затем продолжила обучение в Университете Халла, где получила докторскую степень, занималась важными научными исследованиями в области биохимии и генетики.
После получения докторской степени Гилберт работала научным сотрудником Brewing Industry Research Foundation, сотрудничала с Leicester Biocentre, Delta Biotechnology и лабораторией Адриана Хилла. Она также читала лекции по вакцинологии в Оксфордском университете и стала профессором Института Дженнера в 2010 году.
Спутник V
Российская комбинированная векторная вакцина для профилактики новой коронавирусной инфекции Covid-10 была разработана Национальным исследовательским центром эпидемиологии и микробиологии имени Н. Ф. Гамалеи, директором которого является Александр Леонидович Гинцбург.
Александр Гинцбург — советский и российский микробиолог, академик РАМН и РАН. В 1974 году профессор окончил биолого-почвенный факультет МГУ в Москве, а затем аспирантуру ВНИИ генетики и селекции промышленных микроорганизмов, получил степень доктора биологических наук. В настоящее время Александр Гинцбург является одним из ведущих специалистов в области молекулярной биологии и генетики патогенных микроорганизмов в России, а также автором более чем 300 научных трудов, в том числе двух монографий.
Ученый является руководителем лаборатории генной инженерии патогенных микроорганизмов НИИЭМ им. Н.Ф.Гамалеи РАМН и заведующим кафедрой инфектологии медико-профилактического факультета послевузовского профессионального образования Московской медицинской академии им. И. М. Сеченова.
Covaxin
Весной 2020 года индийская биотехнологическая компания Bharat Biotech International Limited объявила о сотрудничестве с американской компанией FluGen и Университетом Висконсин-Мэдисон (США) в работе над вакциной от Covid-19. Испытания вакцины Covaxin прошли летом 2020 года, на сегодняшний день создано уже более 20 млн. доз, а за 2021 год компания планирует создать еще свыше 700 млн. доз вакцины. Между тем, компания уже заявила о разработке еще более эффективной вакцины совместно с медицинской школой Вашингтонского университета.
Во главе Bharat Biotech International Limited стоит доктор Кришна Элла. Он начал свое образование в Университете сельского хозяйства в Индии, после чего переехал в США. За рубежом Элла получил степень магистра в Гавайском университете, а затем степень доктора наук в Университете Висконсин Мэдисон. После работы в Медицинском университете Южной Каролины в 1997 году Элла вернулся в Индию и основал компанию Bharat Biotech International Limited, которая специализируется на вакцинах и биотерапевтических средствах.
Программы по иммуналогии
Программы по микробиологии
Программы по эпидемиологии
Где учиться на эпидемиолога за границей?
Образование и коронавирус: как учиться за рубежом онлайн?
Несмотря на широкое применение неспецифических профилактических мер и мероприятий, разработка вакцин и широкая вакцинация населения против коронавируса COVID-19, позволяющая сформировать коллективный иммунитет, остается основным способом в борьбе с пандемией и главным средством контроля за ее распространением. По сути, вакцина от коронавируса сегодня какой-либо альтернативы не имеет.
Как работает и действует вакцина
Вакцины представляют собой биологические препараты, которые при введении в организм человека формируют «иммунологическую память» путем выработки Т-лимфоцитов, В-лимфоцитов или антител к возбудителю.
Действие вакцины от коронавируса заключается в создании условий для выработки антител в организме к вирусу SARS-CoV-2 за счет введения в организм ослабленного инфекционного агента. Таким образом, суть вакцины от коронавируса —выработка антител против инфекционного агента (антигена) с целью формирование адекватной иммунологической реакции при его попадании в организм, что позволяет предупредить развитие заболевания или протекание его в легкой форме.
Срок действия прививки от коронавируса зависит от уровня антител и может сохраняться на определенный период, после чего для поддержания достаточного уровня антител требуется ревакцинация. Однако эффективность вакцины у каждого человека может быть различной, что определяется возрастом, индивидуальной спецификой особенностей иммунитета, состоянием здоровья.
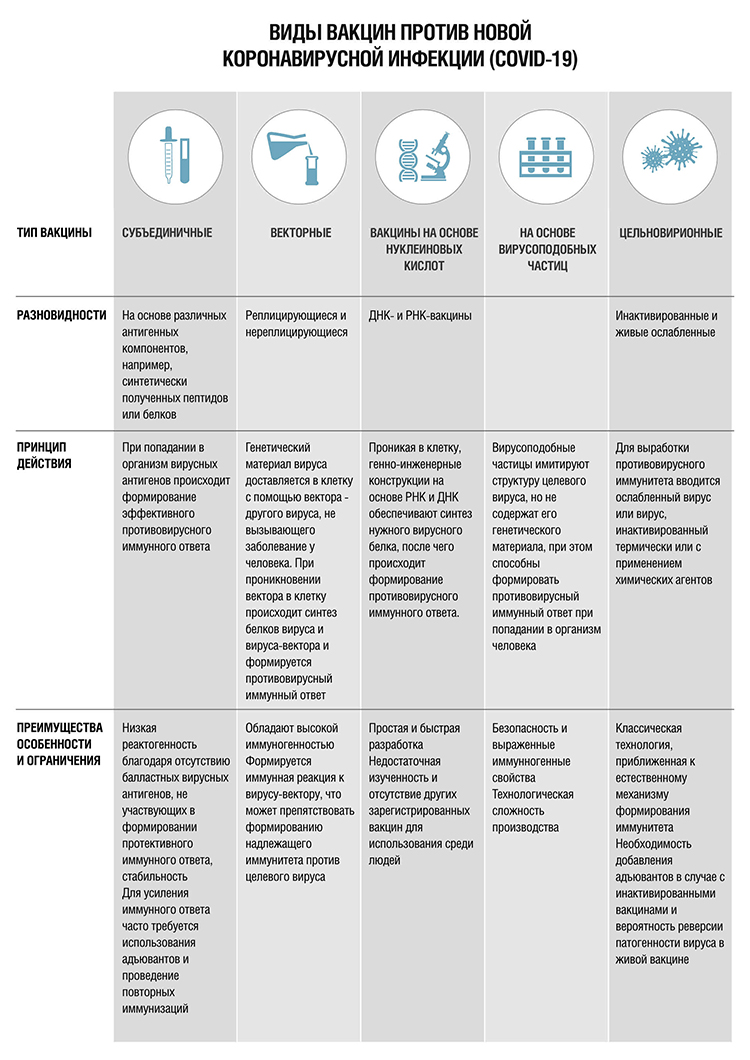
Существующие виды вакцин
Существуют различные технологические платформы, позволяющие создавать различные виды вакцин, каждая из которых имеет определенные преимущества и недостатки:
- Субъединичные (адъювантные, пептидные)
- Векторные
- На основе нуклеиновых кислот (мРНК/ДНК-вакцины)
- На основе вирусоподобных частиц
- Цельновирионные (живые ослабленные и инактивированные)
- Расщепленные (сплит-вакцины)
- Виросомальные
- Химические
- Рекомбинантные
- Поливалентные
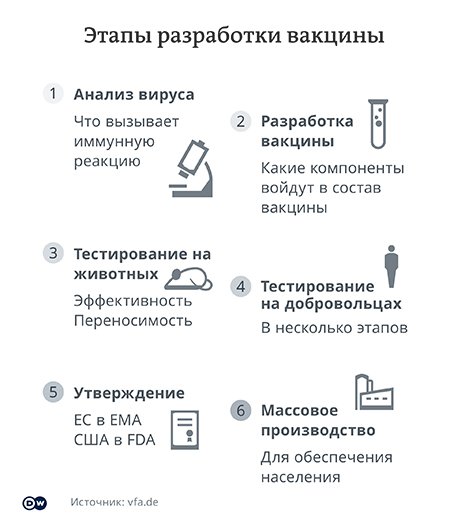
Процесс разработки вакцин
Разработка вакцин — достаточно сложный многоэтапный процесс, который осуществляется на различных технологических платформах с использованием современных биотехнологий.
После создания вакцины препарат проходит тест на его способность индуцировать иммунный ответ (иммуногенность), определяется профиль безопасности, клиническая/эпидемиологическая эффективность и оптимальная эффективная доза вводимого препарата, в том числе способ и кратность введения, срок действия, потребность в ревакцинации и общая схема вакцинации. После завершения полного цикла клинических испытаний вакцины от коронавируса создается технология выпуска вакцины и начинается ее промышленный выпуск.
Сколько вакцин от коронавируса существует
Разработкой вакцины от коронавируса в мире занимается множество компаний. Практически все экономически развитые страны объявили о своем участии в процессе ее создания и для многих из них первенство в создании вакцины стало национальным приоритетом.
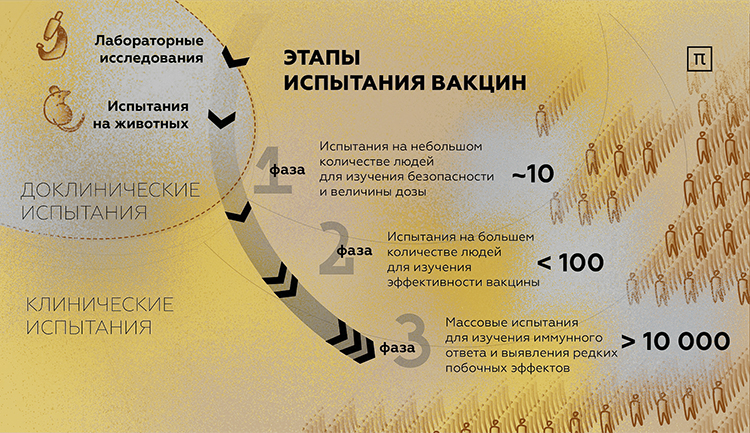
По состоянию на январь 2021 года в мире создано 72 вакцины-кандидата. Однако, поскольку в своем большинстве компании разрабатывающие вакцины еще не прошли все этапы клинических исследований, в частности 3 стадию (рандомизированного, многоцентрового, двойного слепого, плацебо-контролируемого исследования) или находятся на этой стадии, то достоверные данные о них пока отсутствуют, так как лишь полностью проведенные клинические исследования могут подтвердить безопасность и эффективность препарата, а также получить данные о его иммуногенности.
Несмотря на успешное тестирование препаратов на первых стадиях, ряд разработчиков вынужден прекращать их разработку из-за неожиданного побочного эффекта. Так, например австралийская вакцина от ковида, разработанная производителем вакцин CSL совместно с Университетом Квинсленда была снята с производства по причине того, что антитела у вакцинированных лиц затрудняют диагностику ВИЧ и зачастую дают ложноположительные результаты тестов на ВИЧ от вакцины на COVID.
Тем не менее, к концу 2020 года уже определились страны-лидеры и компании-производители вакцин.
Сколько вакцин от коронавируса разрабатывается в России?
По состоянию на декабрь 2020 года в России в 17 научных центрах в разработке находятся 26 вакцин против COVID-19, две из которых уже зарегистрированы.
Новосибирская компания «Вектор», как свидетельствуют последние новости о вакцинах от коронавируса, начинает проводить доклинические испытания новой вакцины, разработка которой проводится на основе вируса гриппа, что позволит защитить население как от гриппа (сезонного), так и против COVID-19.
Также можно отметить вакцину, разрабатываемую в Санкт-Петербургском НИИ вакцин и сывороток ФМБА России, которая прошла этап доклинических скрининговых исследований.
Какие вакцины от коронавируса уже зарегистрированы
Есть ли вакцина от коронавируса, которой уже можно вакцинироваться? Список зарегистрированных вакцин в мире пока небольшой, однако высокие темпы их разработки и значительное инвестирование в эту отрасль позволяют уверенно предположить, что количество вакцин в нем будет быстро пополнятся.
- Первая вакцина от коронавируса зарегистрирована в России — Гам-КОВИД-Вак (Спутник V) (зарегистрирована в августе 2020 года).
- В декабре 2020 года была зарегистрирована FDA (медицинским регулятором Минздрава США) антиковидная американская вакцина BNT162b2 (мРНК-вакцина), разработанная совместно компаниями Pfizer (Пфайзер, ошибочно называемой Файзер ) США и «БайоНТек» (немецкая компания).
- О регистрации своей вакцины mRNA-1273 заявила американская фармацевтическая компания Moderna (Модерна). Более того, компания направила в европейское агентство по лекарственным средствам и регуляторные структуры других стран (Великобритании, Японии, Канады, Австралии и др.) данные доклинических и клинических испытаний относительно безопасности и эффективности вакцины mRNA-1273, многие из них уже одобрили ее применение.
- Практически получено разрешение на использование вакцины AstraZeneca в Евросоюзе, разработанной компанией AstraZeneca (Астразенека) совместно с Оксфордским университетом, а Великобритания с 4 января уже стала первой страной, начавшей ее использовать.
- В Китае зарегистрирована и выдано разрешение CNBG (государственной биотехнической группе), контролируемой фармацевтической компанией Sinopharm на производство и поставки на рынок вакцины от коронавируса, однако китайская вакцина предназначена для вакцинации групп лиц с «высоким риском».
Зарегистрированные вакцины от коронавируса западного производства имеют преимущественно буквенно-цифровую кодировку, что не совсем удобно. Предположительно название вакцины от коронавируса производства компании Moderna будет «СпайкВайс», а вакцины Pfizer/BioNTech — предположительно «Ковьюити», «Комирнати» или «Ковимерна».
Вакцина Гам-КОВИД-Вак (Спутник V)

Зарегистрирована в России 11.08.2020 (временное удостоверение) после проведения первых 2 этапов клинических исследований и получения положительных результатов. В настоящее время проводится третья фаза клинических испытаний, в которой кроме России участвуют Белоруссия, Венесуэла, ОАЭ, Индия и ряд других стран.
Установлено, что из более 20 тыс. добровольцев пострегистрационных испытаний вакцины Гам-КОВИД-Вак лишь 273 участника испытаний заразились коронавирусом, что составляет около 1,5% от всех привитых лиц.
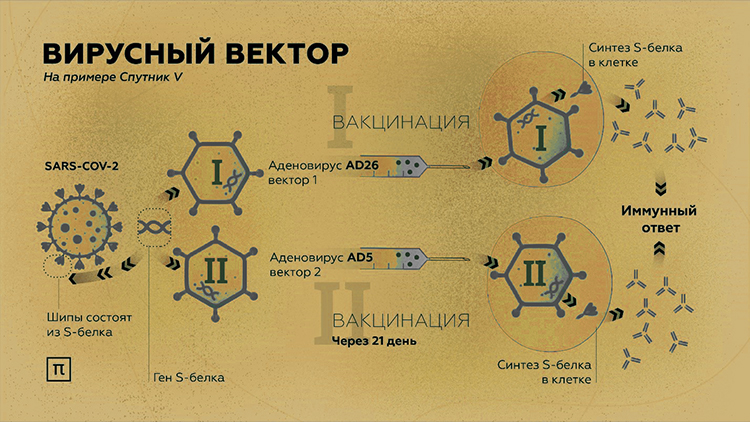
Как работает «векторная» вакцина и кто ее изобрел?
Аденовирусы – это хорошо изученная и давно используемая платформа для создания вакцин с подтвержденной безопасностью. Кто разработал вакцину? Разработчиком вакцины является институт имени Н.Ф. Гамалеи, который работает с вакцинами на основе аденовирусных векторов уже на протяжении многих лет (с 1980 годов) и является лидером в разработке вакцин такого рода, в частности, вакцин против ближневосточного респираторного синдрома и лихорадки Эбола.
Понятие «векторная вакцина» означает, что в роли носителей, доставляющих генетический материал в клетку, выступают векторы, которые создаются на основе другого вируса (в случае коронавируса — на основе рекомбинантных частиц аденовируса человека). То есть, основной принцип создания вакцины — удаление генетического материала аденовируса и введение в геном материала с кодом белка, копирующего S-белок коронавируса (spike-protein), который для организма человека опасности не представляет, но помогает иммунной системе вырабатывать антитела против вируса SARS-CoV-2, эффективно защищающие от инфекции.
Из чего состоит вакцина?
В состав вакцины от коронавируса входят генетический материал вируса SARS-CoV-2 и вспомогательные вещества. Генетический материал в составе вакцины Спутник V представлен геном белка S-шипа SARS-CoV-2 на основе аденовируса человека 26/5 серотипов. Вспомогательные вещества представлены этанолом, сахарозой, полисорбатом, гексагидратом хлорида магния и химическим соединением «Трис».
Как действует вакцина?
Прививка взрослым выполняется дважды: первая — в день первичного обращения при отсутствии противопоказаний, вторая прививка — через 21 день. Дозы вакцины от коронавируса — 0,5 мл в первый и второй раз. Двукратное введение формирует длительный иммунитет. Если говорить о вакцине Гам-КОВИД-Вак, двукратное введение создает защиту по мнению разработчиков до двух лет. Это предположение основано на данных о вакцине от вируса Эбола, которая разработана по такой же технологии, поэтому — нуждается в дальнейших исследованиях и доказательствах. У каждого пациента эффективность вакцины проявляется по-разному – это зависит от особенностей иммунитета, возраста и здоровья человека.
Русская версия вакцины имеет существенную особенность в виде двухкомпонентности, что обуславливает проведение двухэтапной иммунизации человека двумя разными типами аденовируса: вначале используется в качестве вектора аденовирус-26, а через 21 день проводится вакцинация повторно вторым компонентом, созданного на основе аденовируса-5. Такая схема прививки Спутник V позволяет решить проблему низкой эффективности аденовирусных вакцин у людей, имеющих антитела к наиболее распространенным аденовирусам.
Ожидается, что векторная вакцина Гам-КОВИД-Вак позволит формировать иммунитет сроком на два года. Хранение комбинированной вакцины от ковида и процесс ее доставки осуществляется при температуре не выше минус 18°С в местах, защищенных от света. На использовании в качестве вектора аденовирусов разрабатываются и вакцины в других страх: вакцина ad-5-ncov от COVID-19 (Китай), AstraZeneca (Великобритания).
Согласно полученным данным, конечная эффективность вакцины Гам-КОВИД-Вак составляет 91,4%, а при тяжелых случаях эффективна в 90%. При этом, по мнению ее разработчиков пик иммунного ответа на инфекционный агент приходится на 42-й день после введения первого вектора, то есть, будет наблюдаться постепенное усиление иммунного ответа в связи с чем защитная эффективность вакцины Спутник V от коронавируса изменится в сторону увеличения.
Сколько человек сделали прививку и сколько доз произведено?
В настоящее время российская вакцина от COVID-19 Гам-КОВИД-Вак уже широко используется в России для вакцинации населения.
Массовая вакцинация гражданского населения в России началась уже с 5 декабря 2020 года и на середину января 2021 года прививки от ковида получили около 1,6 млн. человек. На сегодняшний день производство вакцины от коронавируса в России пока отстает от ее реальной потребности, что снижает темпы вакцинации населения, особенно страдают поставки вакцины в отдаленные регионы страны.
Производство вакцины от коронавируса в промышленных объёмах осуществляется компанией «Генериум» «Биннофарм» и «Биокад», общая мощность которых не превышает 1,2 млн доз в месяц, что явно недостаточно. В январе в Москве анонсировано открытие совместного предприятия правительства города с компанией «Р-Фарм» по производству Гам-КОВИД-Вак. Завод мощностью 10 млн доз в месяц осуществит первые поставки уже в конце января 2021 года, что позволит в 2021 году провакцинировать значительную часть населения России, тем самым сформировать устойчивый долгосрочный коллективный иммунитет от COVID-19 у значительной части населения и существенно снизить темпы развития и масштабы пандемии.
Кроме того, достигнута предварительная договорённость о создании производства вакцины на зарубежных специализированных предприятиях Бразилии, Индии, Южной Кореи, Китая, что позволит увеличить производительность до 30 млн вакцин в месяц. В РФПИ озвучена информация, что заявки на закупку Гам-КОВИД-Вак в общей сложности на 1,2 млрд доз уже получили из 50 стран.
Лайт-вакцина
Как сообщают последние новости, в России получено разрешение на начало клинических испытаний «лайт-версии» вакцины Спутник V, что в условиях недостатка двухкомпонентной вакцины позволит снизить волну заболеваемости/смертности. Принцип действия лайт-версии аналогичен полноценной вакцине. Ее особенностью является наличие одного из двух компонентов Спутник V. Она также будет безопасна, однако после введения лайт-вакцины иммунитет будет сохраняться менее длительно, предположительно в течение трех-четырех месяцев. При этом, в случае заболевания, привитого коронавирусом, оно будет протекать в легкой форме.
Кому будут делать этот вариант вакцины? Эта версия вакцины эффективна для лиц молодого возраста, возраст которых составляет 14-18 лет. Для лиц пожилого возраста (старше 60 лет) эта версия вакцины не рекомендована. При необходимости после введения лайт-вакцины пациенту может быть введен второй компонент Спутник V через три месяца, тем самым продлив защиту организма.
Когда будет готова эта версия? Предположительно полное исследование и сроки завершения всех испытаний должны быть ограничены периодом этого года.
Куда делают прививку и больно ли ее делать?
Прививку делают внутримышечно в область верхней трети плеча снаружи и выполнение ее не болезненнее, чем внутримышечная инъекция. После введения вакцины человек находится под наблюдением в течение получаса.
Вакцина ЭпиВакКорона
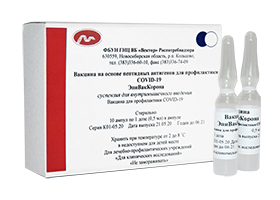
Это рекомбинантный белковый препарат, который содержит искусственно синтезируемый «шип» коронавируса, идентичный натуральному, на который и вырабатываются антитела. Препарат разработан на основе синтетических пептидов и не содержит какие-либо фрагменты, потенциально вызывающие нежелательные реакции, то есть вакцина полностью синтетическая. Препарат, после двукратного внутримышечного введения с интервалом 14-21 дней, индуцирует защитный иммунитет против SARS-CoV-2. Требуется ревакцинация один раз в три года. Преимуществом пептидной вакцины ЭпиВакКорона является практическое отсутствие каких-либо побочных эффектов, что позволяет делать прививки пожилым людям, аллергикам, лицам с хроническими заболеваниями и ослабленной иммунной системой. Не менее важным качеством этого препарата является непритязательность к условиям хранения (хранится при температуре обычного холодильника) и ее транспортировке (при температуре 2 — 8 °С).
Вакцина КовиВак
Еще один препарат — вакцина КовиВак института М. П. Чумакова (цельновирионная инактивированная вакцина на основе «убитого» SARS-CoV-2). Было получено разрешение МЗ России на проведение клинических испытаний (вторая фаза) с участием 200 добровольцев, вакцина прошла регистрацию 20 февраля 2021 года. Это уже 3-я вакцина, проходящая стадию клинических исследований.
Как сообщает Центр Чумакова, по полученным данным вакцина КовиВак от коронавируса позволяет создать эффективный иммунитет от коронавируса с сохранением иммунного ответа на срок от 12 месяцев и более лет. При этом, центр имени Чумакова имеет свое достаточно крупное производство, позволяющее выпускать около 10 миллионов доз в год с перспективой его быстрого расширения.
Вакцина BNT162b2 производства BioNTech/Pfizer
Препарат успешно прошел сертификацию как в США, так и Европейском агентстве (EMA) лекарственных средств, которое допустило препарат к использованию. Вакцина от коронавируса Pfizer вводится в виде двух доз с промежутком в 21—28 дней. Сколько людей участвовали в исследовании? Клинические испытания вакцины проводились на 43,5 тысячах испытуемых, из которых 50% получали плацебо. Серьезных побочных действий у испытуемых (40% из них лица от 56 до 85 лет) не выявлено.

Какие страны купили вакцину? На сегодняшний день вакцину заказали:
- США –100 млн доз первоначально с возможностью дополнительной покупки 500 млн доз.
- Евросоюз – 200 млн с последующей возможностью дозаказа дополнительных 100 млн доз.
- Великобритания – 40 млн доз.
- Япония – 120 млн.
- Канада — 80 млн доз.
- Также, многие страны, закупившие вакцину в крупных объемах расположены в Южной Америке и Азиатско-Тихоокеанском регионе.
В 2021 году Pfizer/BioNtech планируют довести объем производства вакцин до 2 миллиардов доз в год.
Вакцина mRNA-1273 производства Moderna
Вакцина Moderna зарегистрирована в США, Европейском союзе, Японии, Франции, Германии Великобритании, Канады, Австралии Бельгии, Нидерландах и других странах, которые одобрили и начали вакцинацию своего населения этой вакциной. Эффективность вакцины составляет 94,5%, а для лиц старше 65 лет этот показатель превышает 95%.
Кто производит и где производят? Производители вакцины расположены в США и Швейцарии (концерн Lonza). Логистику осуществляет швейцарская компания Kuehne+Nagel, которая имеет специализированный транспорт для перевозки вакцины, условия хранения и доставки которой должны осуществляться при температуре -20 0С.
Вакцина AZD1222 производства AstraZeneca
На стадии завершения регистрации в Евросоюзе и Великобритании находится и векторная однокомпонентная вакцина AstraZeneca (условное обозначение AZD1222), разработанная фирмой AstraZeneca совместно с Оксфордским университетом.
Препарат создан на основе аденовируса шимпанзе. Предусмотрено двухкратное вакцинирование с перерывом в 28 дней. Применение вакцины от коронавируса на основе аденовируса шимпанзе потенциально может быть более эффективной для лиц, уже имеющим иммунитет к аденовирусам человека. По предварительным данным условия хранения вакцины благоприятные и составляют до 6 месяцев при температуре 2 — 8 0С.
Какая вакцина от коронавируса лучше
Понятие «лучшая вакцина от коронавируса» весьма условное и зачастую политизировано. Сравнение уже зарегистрированных и находящихся на регистрации вакцин, попытка определить чья эффективнее, а также выстроить их рейтинг на основании заявленных производителем вакцин данных — некорректно по целому ряду причин.
Прежде всего, несмотря на высокую заявленную эффективность вакцин от коронавируса, полученную в процессе эксперимента его результаты нельзя называть реальной «эффективностью», поскольку при массовой вакцинации во всей популяции эти показатели необязательно сохранятся, то есть эти цифры могут являться неокончательными.
| Moderna | Pfizer | |
| Всего участников | 30000 | 43998 |
| (из них плацебо) | 15000 | 21999 |
| Заболело | 95 | 170 |
| (из них в группе плацебо) | 90 | 162 |
| Эффективность | 94,5% | 95% |
По сути, это ориентировочная информация об испытаниях, без учета отдаленных результатов, позволяющая получить разрешение на регистрацию препарата и использования вакцины в популяции. Ориентировочно лишь через год или полтора после выхода вакцины в популяцию можно оценивать реальную эффективность вакцины от коронавируса.
Важным вопросом является и отсутствие подтвержденных данных о периоде сохранения иммунитета после использования той или иной вакцины, соответственно, потребности и частоте ревакцинации пациента.
Чем отличаются вакцины?
Немаловажным аргументом для сравнения является отличие вакцин друг от друга. Базовым отличием является принцип создания вакцин и технологические платформы, на которых они разрабатываются. Это могут быть как классические технологии (вакцина Гам-КОВИД-Вак на основе аденовируса человека, вакцина КовиВак и китайская Sinovac на основе инактивированного SARS-CoV-2), так и революционные технологии (на основе матричной РНК, использованные в вакцинах компаний Pfizer и Moderna и др.). Каждая из технологий имеет свои преимущества и недостатки.
Чрезвычайно важным вопросом является и возможность промышленного выпуска вакцин на многих производственных объектах в достаточном объеме, а также требования к логистической цепочке (условиям доставки и хранения препарата).
Поэтому, оптимальным вариантом является наличие большого количества зарегистрированных вакцин с возможностью их свободного выбора с учетом эффективности препарата, специфики хранения и доставки до конечного потребителя, ее стоимости, получения в требуемом объеме в краткие сроки. То есть, каждая новая вакцина от коронавируса расширяет возможность использовать вакцины различных производителей, что при условии их присутствия на рынке в достаточных объемах позволит достичь уровня иммунизации населения в мире в 60-70%, что создаст возможность реального контроля за пандемией.
В таблице перечислены отличия основных уже зарегистрированных вакцин:
| Pfizer-BioNTech (США/Германия) | Moderna (США) | Гам-КОВИД-Вак (Россия) | AstraZeneca (Великобритания/Швеция) | |
| Эффективность | 90-95% | 94,5% | 92-95% | 70-90% |
| Цена (за одну дозу) | $20 | $35-37 | $13 | $4-5 |
| Условия хранения | при -80 °C | при -20 °C | не требует особых условий | при -8 °C |
Новые мутации. Снижение эффективности вакцин
Коронавирус активно мутирует и появление новых мутаций является естественным процессом, который будет постоянно продолжаться. Большинство мутаций, которые выявлены на сегодняшний день, являются нейтральными, то есть, они не усилили, но и не ослабили вирус. Однако, ситуация усложнилась с выявлением нового штамма коронавируса в Великобритании (неофициальное название — N501Y или VOC 202012/01) в декабре 2020 года. Данный штамм отличается чрезвычайной заразностью — он быстрее размножается и распространяется, легко передаваясь от человека к человеку. Установлено, что он по разным данным на 56—70% заразнее ныне существующего.
Новый штамм молниеносно распространился по Великобритании и такую же мутацию вируса обнаружили в Нидерландах, Австралии, Дании, Италии. «Британская» мутация вируса наиболее заразна для молодых лиц — это дети и подростки до 19 лет. Уже 23 декабря 2020 года власти Великобритании сообщили о том, что обнаружен еще один штамм коронавируса, завезенный из ЮАР. Предполагается, что новые мутации вируса будут более заразными, но будут представлять меньшую опасность для здоровья и жизни людей. В течение новогодних праздников «британский» штамм «перекочевал» и в Россию.
Мутировавшие варианты вируса без сомнения вызовут вторую волну заболеваемости коронавирусом в мире уже в ближайшее время или осенью 2021 года, однако она будет мягче и слабее нынешней. Как считают многие исследователи, повышенная трансмиссивность нового «британского» штамма SARS-CoV-2, имеющего 23 вида разных мутаций может привести к существенному росту заболеваемости, в связи с чем в 2021 году количество госпитализаций и смертей от COVID-19 будет выше, чем в 2020. Однако убедительных данных того, что этот штамм вызывает более тяжело протекающие заболевания, чем ранее существовавшие варианты нет, поскольку доказательств того, что мутации оказывают серьезное влияние на структуру вируса не найдено.
Поскольку известные на сегодняшний день мутации на строении возбудителя не отражаются, то по мнению ученых зарегистрированные вакцины для профилактики COVID-19 будут эффективны и вакцинный иммунитет не пострадает. Это касается как российской вакцины Гам-КОВИД-Вак, так и вакцины производства BioNTech/Pfizer, которая сохраняет эффективность по отношению к ключевой мутации N501Y у новых вариантов коронавируса, получивших широкое распространение в Великобритании и Южной Африке. Более того, по словам Угур Шахин (главы BioNTech Ugur Sahin), даже в случаях, если возникнет необходимость разработки нового препарата против мутировавшего вируса, технически это можно сделать ориентировочно за шесть-восемь недель.
Безопасность вакцин и риски вакцинации
Есть ли вакцина от коронавируса полностью безопасная для человека и если нет, то когда появится? Практически любая действующая вакцина от коронавируса имеет приемлемый профиль безопасности и в целом, по мнению ВОЗ сертифицированные вакцины являются безопасными. В противном случае они к использованию бы не были допущены. Тем не менее, существует множество публикаций, в которых указывается что от вакцины от коронавируса умерло уже несколько человек, то есть люди умирают в процессе вакцинации. Однако эти данные не совсем корректны.
Действительно в ходе клинических испытаний вакцин-претендентов от коронавируса зарегистрировано несколько случаев смерти среди нескольких десятков тысяч добровольцев, однако, тщательно проводимое изучение таких случаев показало, что все случаи смерти происходили по независящим от прививок причинам. Основными причинами летальных исходов, которые нельзя никак связать с вакциной были: инфаркт миокарда, инсульт, автомобильные аварии, обострение хронических заболеваний и др. причины, независимые от вакцинации. То есть, непосредственно умерших от вакцины от коронавируса среди лиц, проходящих испытание препаратов нет. Также нужно учитывать, что люди умирают как в группе принимающих вакцину, так среди лиц, принимающих плацебо. Поэтому не стоит, переживать, что при проведении массовой вакцинации возможен летальный исход.
В то же время, как показали исследования, применение вакцины от коронавируса не исключает развитие побочных реакций, которые в большинстве случаев протекают легко (невысокая температура, гриппоподобный синдром, общее недомогание, боли в мышцах, краснота/отек/болезненность в зоне укола), которые обычно проходят в течение 2-3 суток. Случаи тяжелых побочных эффектов (аллергический шок, обострение хронических заболеваний и др.) чрезвычайно редки.
Стоит ли делать прививку, подвергая себя риску?
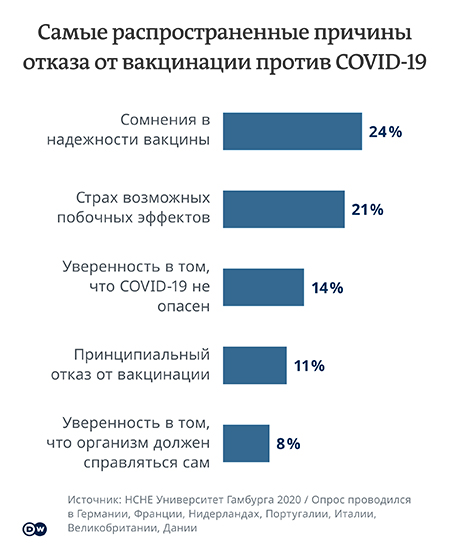
Многие люди во всем мире ждут, когда начнут проводить массовую вакцинацию и когда можно будет сделать прививку от коронавируса. Некоторая часть людей сомневаются поможет ли она и опасаются развития побочных эффектов от вакцины. Определенная часть мирового общества считает, что вакцина опаснее ковида и категорически не согласны прививаться. Такое расслоение общества обусловлено противоречивой информацией и дискуссиями в социальных сетях, в которых активно обсуждают преимущества и отличия вакцин, делятся данными анализов с титрами антител. Уровень доверия в целом со стороны общества в большинстве стран мира к процессу вакцинации остается низким. Ниже указаны наиболее частые причины отказа от проведения вакцинации.
В начале декабря 2020 года (с момента начала массовой вакцинации) перед россиянами также остро встал вопрос делать ли прививку? К сожалению, среди российских граждан доверие к вакцине также невысокое — 58% опрошенных лиц пока прививаться от COVID-19 не готовы даже бесплатно (по данным опроса «Левада-центра»). Определенная группа россиян готовы вакцинироваться лишь западными вакцинами компаний Moderna, Pfizer, AstraZeneca.
Какие прививки делают В Москве? В настоящее время в РФ лишь одна действующая вакцина от коронавируса. Привиться пока можно только одной вакциной – Гам-КОВИД-Вак (Спутник V). Какая-либо импортная вакцина в России в настоящее время не зарегистрирована и для вакцинации не используется. Кому будут делать вакцину? Массовая вакцинация проводится всем лицам, на принципе добровольности, а также людям старше 60 лет.
Решение делать или не делать прививку каждый гражданин должен принимать самостоятельно, исходя из состояния своего здоровья, взвесив пользу и возможный риск. В целом, вероятность заболеть коронавирусом существенно превышает риск развития побочных явлений при вакцинации.
Доступность вакцин
Несмотря на декларацию лидеров стран G20 «не жалеть усилий» для обеспечения справедливого распределения вакцин от COVID-19 в настоящее время большую часть зарегистрированных вакцин от коронавируса закупили богатые страны. Вакцинация населения безопасными и эффективными вакцинами сейчас проводится в 42 странах, при этом, из них высокий уровень доходов имеют 36 и средний доход —6 стран. То есть, государства с низким/средним уровнем дохода вакцину от коронавируса не получают. Богатые страны, в которых проживает всего 14 процентов населения мира, уже обеспечили своих граждан 53 процентами зарегистрированных вакцин. Практически все вакцины Pfizer/Moderna, несмотря на их относительную дороговизну купили западные страны. В то время как доступ для стран с низкими доходами из-за их цены и особых требований к их логистике будет затруднен.
В настоящее время заказы и предзаказы на зарегистрированные и проходящие процедуру регистрации вакцины от ведущих производителей продолжают нарастать и по данным Bloomberg по состоянию на 13.01.2021 года в разрезе стран составляют:
При этом, согласно прогнозам, девять из десяти человек, проживающих в наиболее бедных государствах в 2021 году сделать вакцину не смогут. По состоянию на 8.01 2021 года странами-лидерами процесса вакцинации являются:
- США – 7 млн 52 тыс. доз
- Китай – 4,5 млн доз
- Израиль почти – 1,6 млн доз
- Великобритания – 1 млн 489 млн доз
- Израиль —1млн 090 тысяч доз
- ОАЭ – 941,6 тыс. доз
Более того, как отметил глава ВОЗ, богатые страны вначале скупили большую часть произведенных вакцин, а теперь начинают заключать двухсторонние дополнительные сделки на их поставку, что означает, что население из группы высокого риска в наиболее маргинализированных и беднейших странах вакцину не получат. Такое распределение вакцин из-за высокой миграции населения может крайне негативно сказаться на эффективности глобального процесса вакцинации. И только вакцинация на справедливой основе позволит максимально эффективно стабилизировать ситуацию с пандемией.
По мнению ВОЗ эту проблему необходимо решить с помощью таких организаций как ACT Accelerator, которая объединяет государства и организации, участвующие в производстве и распределении вакцин и COVAX —глобальной инициативы в целях предоставления всем странам мира равноправного доступа к эффективным вакцинам в которой участвуют 172 страны. Необходимо осознать то, что в мире в ближайший год не будет достаточного количества вакцин для предотвращения пандемии.
Показания и противопоказания к проведению вакцинации
Согласно приказу Минздрава РФ от 16 декабря 2020 года вакцинация от коронавирусной инфекции стоит в календаре прививок. Кому можно проводить вакцинацию? Лицам, достигшим 18 лет, не имеющим тяжелых хронических заболеваний и острых инфекционных заболеваний на момент вакцинации. Обязательна ли вакцинация? Часто врачи сталкиваются с заявлением «не хочу делать прививку». В настоящий момент обязательная вакцинация не планируется, она добровольная и решение стоит ли делать прививку от ковид каждый принимает самостоятельно или с лечащим врачом, основываясь на состоянии здоровья. В Минздраве высказываются против вакцинации в порядке приказа — лучшим вариантом является предоставление информации, а человек уже решает сам ставить ли прививку.
Есть определенный контингент, которому вакцинация желательна, но и для них она не будет обязательной. Действительно, в середине октября появились сообщения в сети о том, что медработников в Москве заставляют делать прививку принудительно в то время, когда вакцина находилась на третьей фазе исследований и необходимо было тестирование на добровольцах. С помощью юристов, которые заявили о том, что участие в клинических исследованиях препарата является добровольным, права медиков, которым грозили увольнением, были защищены.
В первую очередь вакцинацию настоятельно рекомендуют проводить медикам и учителям. Нужна ли прививка этому контингенту? Нужна, это необходимо для их безопасности и безопасности лиц, с которыми они контактируют. К приоритету первого уровня также относятся больные хроническими заболеваниями бронхолегочной системы, сердечно-сосудистой системы и сахарным диабетом. Нужна ли прививка этому контингенту? По наблюдениям при диабете имеются высокий риск развития COVID-19 в тяжелой форме и со смертельным исходом. Специалисты считают, что диабетикам вакцина против коронавируса должна быть предоставлена в приоритетном порядке. Больные сахарным диабетом имеют более высокий риск (в 3-4 раза выше) госпитализации с COVID-19 и протекает он особенно тяжело. Вакцинация же может снизить заболеваемость и смертность больных с диабетом от COVID-19. К приоритетам второго и третьего уровня отнесены социальные работники, полицейские, работники торговли и общественного транспорта, работники гостиниц, банков и парикмахерских, студенты и призывники.
Начиная с 7 декабря 2020 г, в Москве и Подмосковье врачам делают прививки. Медицинские учреждения проводят запись на прививку среди своих сотрудников и передают их в прививочный кабинет поликлиники — вакцинация проводится только в государственной поликлинике, которая получает препарат. Перед вакцинацией все сдают кровь на антитела и ПЦР-мазки (на получение результатов уходит двое суток). Если ПЦР отрицательная и антител нет, формируют группу. Перед прививкой предстоит осмотр терапевта. После прививки выдается справка о прививке от коронавируса, которая может понадобиться для авиаперелетов, если будут изменены правила обслуживания авиапассажиров международных рейсов.
На сегодняшний день вакцина выдается медицинским учреждениям бесплатно для вакцинации лиц групп риска, о которых говорилось выше. По мере наращивания производства, вакцинация будет доступна всем желающим.
Делать ли вакцину от коронавируса маленьким детям? Вакцинация детям не рекомендуется, поскольку в настоящий момент нет исследований по безопасности вакцины для детского возраста. Кроме того, дети не входят в группу риска по данной инфекции, болеют редко и переносят ее легко и без осложнений.
Ограничения к вакцинации имеются при хронических заболеваниях, но в каждом конкретном случае вопрос решается врачом в соответствии с состоянием здоровья пациента и возможных рисков. Противопоказания на вакцину Спутник V не разрешают делать прививку пациентам с выраженными нарушениями функции почек, печени, сердечно-сосудистой системы, заболеваниями ЦНС.
Список заболеваний, кому нельзя проводить вакцинацию, включает:
- хроническую болезнь почек с хронической почечной недостаточностью;
- гепатиты В, С, цирроз печени с печеночной недостаточностью;
- туберкулез, сифилис, ВИЧ;
- тяжелые аллергические реакции в прошлом.
Прививку нельзя делать лицам, перенесшим в течение текущего года инфаркт миокарда, эндокардит, миокардит или имеющим декомпенсированный сахарный диабет.
Противопоказания на прививку от ковид взрослым включают также тяжелые заболевания органов кроветворения. Прививка противопоказана лицам с острым нарушением мозгового кровообращения в течение текущего года.
Любое инфекционное заболевание — это противопоказание для вакцинации.
Вакцинацию на проводят беременным, кормящим и женщинам, планирующим беременность в течение трех ближайших месяцев.
Противопоказания на вакцину от коронавируса имеют лица, страдающие аутоиммунными заболеваниями (красная волчанка, псориатический артрит, аутоиммунный тиреоидит, ревматоидный артрит и другие). Почему нельзя проводить им вакцинацию? Стимуляция иммунной системы может вызвать обострение аутоиммунного заболевания, особенно это касается тяжелых аутоиммунных состояний, угрожающих жизни.
Также, прививку не стоит делать онкобольным. Это связано со стимуляцией иммунитета и возможной стимуляцией онкологического процесса. Проведение лучевой терапии в течение последнего полугодия является противопоказанием к вакцинации.
До какого возраста делают прививку?
С 26 декабря Минздрав РФ разрешил применение Гам-КОВИД-Вак для пожилых. Теперь лица от 60 лет, не имеющие тяжелых хронических заболеваний в стадии декомпенсации, по желанию могут пройти вакцинацию. После того, как вакцина была одобрена для этой возрастной категории, количество прививающихся значительно выросло. Разумеется, что прежде, чем делать прививку пожилым людям, они должны быть тщательно обследованы, поскольку многие лица старше 60 лет имеют хронические заболевания, что существенно ограничивает возможность проведения вакцинации пенсионерам. Окончательное решение о возможности вакцинации данной категории больных принимает врач после обследования и оценки возможных рисков.
Как отказаться от прививки от ковид?
Все состояния и заболевания, о которых говорилось выше, позволяют законно отказаться от вакцинации. Если у человека имеются противопоказания, ему оформляют медотвод от прививки ковид. Есть абсолютный медотвод — тяжелый первичный иммунодефицит и выраженная аллергическая реакция на введение первого компонента вакцины. Есть и временный отвод, связанный с острым респираторным заболеванием или обострением хронического. В этом случае человек может пройти вакцинацию через две-четыре недели, когда состояние его стабилизируется. Во всех остальных случаях отказ пациента от вакцинации не будет иметь оснований, однако он имеет на это право.
Что нельзя после прививки?
После прививки люди должны соблюдать самоизоляцию, поскольку эффективный иммунитет формируется у всех по-разному. Заместитель директора центра им. Гамалеи уточнил, что пик иммунного ответа приходится на 42 день от первой инъекции. Вторым важным условием после прививки является исключение аллергогенных продуктов (цитрусовые, шоколад, яйца, рыба) и посещения сауны или бани. Немаловажным является исключение алкоголя. Сколько нельзя принимать алкоголь? Достаточно воздержаться от него в течение трех дней после прививки.
Как связаны алкоголь и вакцина от коронавируса? Поскольку алкогольные напитки угнетают иммунную систему, поэтому иммунный ответ трудно и некачественно формируется — процедура вакцинации может стать бессмысленной. В связи с этим, появилась первичная информация о том, что весь период вакцинации (42 дня) нельзя употреблять алкоголь, поэтому многие отказывались от нее. Директор НИЦ им. Гамалеи, академик Александр Гинцбург сделал разъяснения и ответил на вопрос сколько нельзя пить? Нельзя принимать алкоголь после введения первого и второго компонента вакцины в течение трех дней. Это является обычной рекомендацией во время проведения любых прививок. Такие же ограничения в отношении алкоголя должны выполняться и перед прививкой — в течение трех дней не пить перед прививкой от ковид.
Можно ли делать прививку переболевшим ковидом?
Делать ли переболевшим прививку и нужна ли переболевшим ковид прививка? Вакцинация от коронавируса не рекомендована если переболел человек и у него определяются антитела IgG к вирусу SARS-CoV-2. Для этого проводится тест на наличие IgG в крови. Почему не делают прививку? Если есть антитела этого класса (показатель IgG более 10), то это свидетельствует о наличии сформированного защитного иммунитета, который сохраняется до полугода. Вакцина от коронавируса переболевшим показана только в том случае, если человек переболел не раньше, чем полгода назад и уровень IgG снизился.
Опасна ли вакцина и заразен ли после прививки человек?
Все вакцины, пошедшие регистрацию, опасности не представляют, а незначительные побочные симптомы быстро проходят. Человек, получивший прививку не является заразным для окружающих лиц.
Последствия и осложнения
Побочные эффекты вакцины от коронавируса развиваются у незначительного числа вакцинированных лиц. Побочные действия прививки могут включать:
- умеренную болезненность в месте инъекции, зуд, припухлость;
- последствия прививки могут проявляться также покраснением в месте введения;
- после вакцинации может кратковременно повышаться температура, возможны заложенность носа, першение в горле как при гриппе или респираторных заболеваниях и общие симптомы в виде ощущения слабости, разбитости, болей в суставах и ломоты в теле.
Все побочные явления развиваются в первые двое суток и имеют легкую или среднюю степень тяжести. Исчезают в течение 2-3 дней самостоятельно, иногда требуется прием жаропонижающих средств и антигистаминных препаратов при выраженной местной реакции. Более серьезные осложнения в виде выраженной аллергической реакции, тошноты, рвоты, увеличения лимфоузлов также встречаются. Могут наблюдаться изменения лабораторных показателей — повышение уровня печеночных трансаминаз, повышение СОЭ, лейкоцитов, лимфоцитов и тромбоцитов, появление эритроцитов в моче. Изменение лабораторных показателей не нуждается в дополнительном лечении.
Где можно сделать прививку от коронавируса
Где сделать вакцину от коронавируса? Совершенно точно, что этим будут заниматься государственные поликлиники, которые будут получать бесплатную для россиян вакцину. Как получить вакцину от коронавируса? По заявлению вице-премьера Дмитрия Чернышенко записаться на прививку от COVID можно будет на Едином портале госуслуг, запись на котором откроется до конца января 2021 г. Там же будут указаны прикрепленные поликлиники и прививочные пункты, в которых можно будет пройти вакцинацию. Поставить вакцину от коронавируса можно после получения добровольного согласия пациента, при наличии паспорта, полиса ОМС, справки с места работы (для подтверждения контакта с большим количеством людей) и студенческого билета для студентов.
Прививка от ковид в Москве проводится в 100 пунктах. Записаться на прививку можно на сайтах mos.ru, emias.info, через мобильные приложения «Моя Москва», «ЕМИАС.ИНФО», «Госуслуги Москвы». Записаться нужно на первую вакцинацию, а на повторную идет автоматическая запись. За сутки до второй вакцинации человек получает СМС-сообщение, в котором указывается дата, время и поликлиника. Вакцина от коронавируса в Москве в первую очередь предоставляется лицам, находящимся в основной группе риска: старше 60 лет, лица с хроническими заболеваниями, работники, которые постоянно контактируют с большим количеством людей. В московской области записаться на прививку можно по номеру 122 или через портал госуслуг. Как сделать вакцину от коронавируса в Санкт Петербурге? В СПб комитет по здравоохранению дал разрешение на публикацию адресов пунктов, в которых проводится вакцинация. Они в свободном доступе в интернете, их 70 и это государственные поликлиники. Наибольшее количество пунктов открыто в Выборгском и Невском районах.
Можно ли платно сделать прививку? Московский департамент здравоохранения предложил включить частные клиники в прививочную работу. Учреждения должны самостоятельно перевозить вакцину со склада с соблюдением температурного режима, а данные о вакцинированных загружать в общую систему ЕМИАС. Врачи клиники также должны провести осмотр до и после вакцинации. Планируется, что частные медучреждения получают вакцину бесплатно, поэтому его стоимость не должна включаться в стоимость услуг. Платная услуга будет только за лабораторные исследования и прием врача перед вакцинацией.
Цена вакцины от коронавируса
В течение нескольких месяцев обсуждался вопрос платная ли вакцина и сколько стоит вакцина от коронавируса в России? Отвечая на вопрос сколько будет стоить вакцина Гам-КОВИД-Вак Министерство здравоохранения РФ уточнило, что отпускная цена Спутник V от производителя составляет 1942 руб. (за два компонента), но для россиян она будет бесплатной за счет государственных средств.
Также, дан ответ на вопрос, где купить вакцину от коронавируса в Москве? Ее нельзя будет купить в аптеках, поскольку она будет поставляться со склада только в прививочные пункты. Однако, людям должны быть доступны несколько вакцин для возможности выбора. Не исключено, что в случае регистрации в России будет закупаться и импортные вакцины, которые будут платными.
Как стать добровольцем для испытания вакцины от коронавируса
В связи с тем, что вакцины будут и дальше создаваться и совершенствоваться, будут необходимы лица, желающие принять участие в испытаниях. Прежде всего пройти испытание могут здоровые лица, достигшие 18 лет. Мы можем рассказать, как приходили испытания вакцины Гам-КОВИД-Вак, первая и вторая фазы клинических испытаний которой завершены 1 августа 2020 г. Как это будет происходить в дальнейшем при испытании других вакцин сказать трудно.
Как приходят испытания? Разработчик вакцины сам клинические испытания не проводит, а описывает необходимые условия исследований и создает протокол исследования с указанием как должно происходить исследование, в какие сроки, сколько потребуется добровольцев, сколько времени нужно за ними наблюдать. С протоколом знакомятся клинические центры — медицинские университеты, клиники, госпиталя и прочие медицинские организации. После этого разработчики заключают договор с клиникой, которая имеет возможность создать все условия для испытаний и согласна принять участие в исследовании.
Поиском добровольцев занимаются клинические центры (чаще всего у них уже есть база добровольцев, которые раньше принимали участие в тестировании препаратов). Испытания вакцины Гам-КОВИД-Вак проходили в Москве. Вакцина в форме лиофилизата (твердая форма) испытывалась на добровольцах в Сеченовском университете, а в жидкой форме — в Военном госпитале имени Н. Н. Бурденко. Добровольцы набирались из уже имеющейся базы участников исследований университета, а в госпитале им. Н. Н. Бурденко — из военнослужащих и гражданских лиц. Когда вакцина проходит третью фазу испытаний, то включаются пациенты с определенной патологией и старшего возраста. Но это возможно лишь тогда, когда профиль безопасности выяснен на здоровых добровольцах. В ходе третьей фазы клинического пострегистрационного исследования принимают участие до 40 000 добровольцев.
Отзывы о вакцине от коронавируса
По состоянию на середину января 2021 года вакцинация проводится преимущественно вакциной Гам-КОВИД-Вак (Спутник V). Если в начале декабря 2020 года вакцинацию прошли больше 100 тысяч человек, то к середине января 2021 количество вакцинированных уже составило 800 тысяч.
Также началась вакцинация ЭпиВакКороной от ГНЦ «Вектор». Ранее глава Роспотребнадзора Анна Попова сообщала, что этот препарат рекомендуется лицам старшего возраста и с хроническими заболеваниями. Это объясняется тем, что препарат синтетический и в нем нет живого белка и фрагментов вируса. Этот препарат подходит для людей с иммуносупрессивными заболеваниями и аллергиков.
Разумеется, что уже появились отзывы тех лиц, кому делали прививку, но форум, посвященный этой теме отсутствует. Наиболее часто отзывы привитых отражают побочные реакции после прививки. В большинстве случаев — это слабость, недомогание, повышение температуры (порой до 38,5 градусов), ломота в теле, тошнота и общая интоксикация. Однако отзывы людей о прививке от ковид не всегда отрицательные. Многие отмечают, что прививка переносилась легко, повышения температуры не отмечалось, было небольшое недомогание и слабость и умеренная болезненность в месте инъекции. Все нежелательные эффекты проходили на третий день. Некоторые отмечают реакцию на вторую дозу, которая перенеслась тяжелее — сильный озноб в течение суток при невысокой температуре.
Мнение врачей о вакцине различается. Некоторых из них удивляет то, что Гам-КОВИД-Вак уже применяется, тогда как результаты третьей фазы испытаний отсутствуют. Многие говорят, что лично они бы не прививались препаратом, не прошедшим третью фазу испытаний. Для специалистов важно, чтобы любой препарат стал применяться после того, как полностью завершится испытание. В первой фазе этот препарат тестировался на небольшом количестве добровольцев и в ускоренном темпе. Ускоренный режим недопустим в подобных случаях. Пока препарат не опробуют на большом количестве добровольцев, невозможно определить, вызывает ли она серьезные осложнения или ухудшает течение имеющихся хронических заболеваний. Это особенно важно для людей старшего возраста. В то же время они не считают, что у вакцины нет шансов на успех и достойно завершить третью фазу испытаний, которая проводится в Объединенных Арабских Эмиратах. Это демонстрирует то, что испытания будут проводиться по правилам ВОЗ и вакцина будет иметь такой же признанный уровень, как и другие подобные препараты.
Список источников
- Hodgson, S. et al. What defines an efficacious COVID-19 vaccine? A review of the challenges assessing the clinical efficacy of vaccines against SARS-CoV02. 2020. Avaliable at: doi.org/10.1016/S1473-3099(20)30773-8 [Last accessed: Nov 16 2020]
- Jeyanathan, M., et al. Immunological considerations for COVID-19 vaccine strategies. Nat Rev Immunol 20, 615–632 (2020). https://doi.org/10.1038/s41577-020-00434-6
- British society of Immunology. Immune responses to viruses. https://www.immunology.org/public- information/bitesized-immunology/pathogens-and-disease/immune-responses-viruses. [Last accessed: Nov 16 2020]
- Гонка престижа за мировое первенство в производстве вакцин против COVID-19 вошла в заключительную фазу. Электронный ресурс: https://www.apteka.ua/article/561898
Россия стала первой страной, где зарегистрирована вакцина от короновирусной инфекции, та самая, созданная совместно специалистами Минобороны и центром Гамалеи. Об этом министр здравоохранения Михаил Мурашко доложил Владимиру Путину на президентском совещании с правительством. Разработки антиковидного барьера ведутся в разных странах, но одобрена — то есть получила регистрационное удостоверение, только у нас.
Раствор для внутримышечного введения находится в двух пробирках красного и синего цветов. На них указаны дата выпуска, срок годности, условия хранения — не допускается хранение размороженного препарата.
«Сегодня утром впервые в мире зарегистрирована вакцина против новой коронавирусной инфекции», — констатировал Владимир Путин.
Соблюдены все формальности, у вакцины даже появилось официальное название — «Спутник V». Аналогия с освоением космоса. В 1957-ом мы первые запустили туда «Простейший Спутник 1», в 2020-ом снова первыми разработали, создали и испытали лекарство от COVID-19.
«У всех добровольцев выработались высокие титры антител COVID-19. При этом ни у кого из них не отмечено серьезных осложнений иммунизации», — заявил министр здравоохранения Михаил Мурашко.
Клинические испытания прошли успешно, вакцина работает эффективно, а главное безопасно. Проверено на дочери президента. Владимир Путин почти никогда не говорит о своей семье, но сегодня выяснилось — в ней тоже нашлись добровольцы.
«Одна из моих дочерей сделала себе такую прививку. Я думаю, что в этом смысле она поучаствовала в эксперименте. После первого укола, после первой прививки температура была у нее 38, на следующий день 37 с небольшим, и все. После второго укола, второй прививки тоже температура немного поднялась, но потом сошла на нет. Чувствует себя хорошо, и титры высокие», — поделился глава государства.
Инъекции две, конечно, потому и ампулы разные. Ставят с промежутком в три недели. Вакцинация бустерная — это когда второй укол усиливает действие первого. Разработка военных медиков Министерства обороны совместно с коллегами из Национального исследовательского центра имени Гамалеи. В прошлом у них уже был опыт сотрудничества и он оказался успешным.
«Именно в совместной работе с учреждением Минобороны, работая над вакциной против вируса Эболы в Африке, удалось доказать, что продолжительность иммунитета при таком использовании вакцины продолжается по крайней мере два года, а может и больше», — отметил директор Национального исследовательского центра имени Гамалеи Александр Гинцбург.
Вакцина от коронавируса создана по такому же принципу, а значит, защитный эффект будет сохраняться также не меньше двух лет. Ученые продолжат клинические исследования препарата — у него не должно оказаться побочных эффектов.
На этот раз к испытаниям привлекут несколько тысяч человек. Параллельно начнется производство вакцины. Сначала центром имени Гамалеи Минздрава России и компанией «Биннофарм». Затем список предприятий будет расширен.
«Конечно, можно ожидать определенных изменений в организме. Но с другой стороны, мы убедились в том, что эти изменения, они кратковременные и вреда никакого не причиняют, кроме того, что этот человек обезопасен», — сообщил президент НМИЦ сердечно-сосудистой хирургии имени Бакулева, академик Лео Бокеря.
Над созданием вакцины против коронавируса работают ученые многих стран мира. Продолжаются исследования и в России, так что в ближайшее время могут появиться новые препараты. Но к тому времени, если потребует ситуация, может начаться вакцинация.
«Очень надеемся, что в сентябре, в конце августа — в сентябре уже начнет появляться вакцина, первой категории для вакцинирования которой станут, как мы надеемся, медицинские работники», — заявила заместитель председателя правительства РФ по вопросам социальной политики Татьяна Голикова.
Следом учителя — они ведь работают с детьми. Всего в России планируют охватить вакцинацией минимум 60 процентов населения и 75 процентов, если речь идет о группах риска.
«Мы должны быть благодарны тем, кто сделал этот первый шаг, очень важный: очень важный для нашей страны, вообще для всего мира. Надеюсь, что мы сможем в ближайшее время начать массовый выпуск этого препарата, с тем чтобы все, кто хочет могли бы воспользоваться разработками и достижениями наших специалистов, наших ученых», — сказал Владимир Путин.
Изобретение запатентовано, информацию о нем направили во Всемирную организацию здравоохранения, чтобы там в общий список вакцин включили и «Спутник V». Интерес к препарату проявляют в ряде зарубежных стран. Два президента — Филиппин и Сербии, Родриго Дутерте и Александр Вучич вызвались на себе испытать эффект российской вакцины от коронавирусной инфекции.
Пандемия коронавируса ,
29 мар 2021, 18:37
Какие вакцины от коронавируса используют в мире
В России массовая вакцинация от COVID-19 началась 18 января. В мире на конец марта прививают население уже в 141 стране. Какие вакцины используют — в обзоре РБК
Вакцина «Спутник V»
«Спутник V», разработанная Центром эпидемиологии и микробиологии имени Н.Ф. Гамалеи, получила госрегистрацию Минздрава в августе. Вакцину зарегистрировали после второй фазы испытаний, а третий финальный этап стартовал в сентябре.
Эффективность «Спутника V» разработчики оценили выше, чем в 95%. Эти данные были получены при исследовании добровольцев, получивших две инъекции препарата. «Спутник V» разработан в двух видах: замороженном (жидкая «Гам-КОВИД-Вак» хранится при температуре не выше минус 18 °С) и лиофилизированном (порошок «Гам-КОВИД-Вак-Лио» хранится при температуре от плюс 2 до 8 °С). Препарат вводится двукратно с интервалом в три недели. В ФАС заявили, что стоимость инъекции «Спутником V» не превысит 1 тыс. руб.
5 декабря Москва стала первым российским регионом, начавшим масштабную вакцинацию «Спутником V», а с 18 января началась массовая вакцинация во всей России. Первой среди зарубежных стран, зарегистрировавших российский препарат, стала Белоруссия. Такое же решение приняли власти Аргентины, Венесуэлы и некоторых других стран
Вакцина Pfizer/BioNTech
Фото: Owen Humphreys / Reuters
Немецкая компания BioNtech разработала вакцину совместно с американской Pfizer. На третьей фазе клинических испытаний препарат показал эффективность на уровне 95%. У вакцины есть обязательное условие использования: ее нужно хранить при температуре не выше минус 70 градусов Цельсия, а после разморозки она пригодна в течение пяти дней. Разработка Pfizer-BioNTech вводится в два приема с промежутком в три недели. Великобритания стала первой страной, одобрившей применение Pfizer и BioNTech, за ней последовали Канада, США и страны Европы и Ближнего Востока. Массовая вакцинация в США и Канаде началась 14 декабря, а в европейских странах — 27 декабря
Вакцина Moderna
Фото: Hans Pennink / AP
Эффективность вакцины американской фармацевтической компании Moderna составила 94,5%, а при тяжелых случаях заболевания — 100%. Вакцину вводят в два приема с интервалом в четыре недели. Препарат можно до 30 дней хранить при 2–8 градусах Цельсия. В этом году Moderna планирует выпустить 600 млн доз.
18 декабря США одобрили использование Moderna и заказали 200 млн доз с возможностью покупки еще 300 млн. Следом разрешение на использование она получила в Канаде, Израиле, Великобритании и Швейцарии. 6 января Европейский регулятор одобрил препарат американского производства
Вакцина AstraZeneca и Оксфордского университета
Фото: Francis Mascarenhas / Reuters
Вакцина, разработанная британской компанией AstraZeneca вместе с Оксфордским университетом, показала эффективность на уровне 70%, а при одном из способов введения (сначала вводят половину дозы, а через месяц — полную) — 90%.
У препарата есть два преимущества: его можно хранить при той же температуре, которую позволяет создать обычный холодильник, а его стоимость составляет $4–5. Вводится два раза с интервалом в 4–12 недель.
Великобритания первой в мире разрешила использовать AstraZeneca и заказала 100 млн доз. Препарат получил разрешение на использование в Индии, Аргентине, Доминиканской Республике, Сальвадоре, Мексике и Марокко.
В марте 2021 года вокруг препарата AstraZeneca разразился скандал. Более 15 стран Европы, в том числе Германия, Франция, Испания, и некоторые страны Азии и Африки частично или полностью отказались от препарата. Такое решение власти приняли на фоне сообщений об образовании тромбов у привившихся и смертельных исходах.
В самой компании указывают на отсутствие доказательств, что к смерти пациентов привела именно вакцинация. 18 марта вышло заключение Европейского агентства лекарственных средств (EMA) о том, что AstraZeneca не увеличивает риски по образованию тромбов. ВОЗ также продолжает рекомендовать использование препарата. После этих заявлений европейские страны, кроме некоторых скандинавских, возобновили иммунизацию AstraZeneca.
Вакцина «ЭпиВакКорона»
Фото: Кирилл Кухмарь / ТАСС
Пептидная вакцина новосибирского научного центра «Вектор» «ЭпиВакКорона» получила регистрационное удостоверение в октябре 2020 года. Она, как и «Спутник V», была зарегистрирована после двух стадий клинических испытаний.
Вакцину вводят двукратно внутримышечно с интервалом в две-три недели. Препарат можно хранить при температуре от 2 до 8 градусов выше нуля. В Роспотребнадзоре отмечают, что вакцина подходит для пожилых и людей с хроническими заболеваниями. В центре «Вектор» заявили, что стоимость препарата будет эквивалента стоимости «Спутника V», то есть около 1 тыс. руб.
Глава Роспотребнадзора Анна Попова сообщала, что «ЭпиВакКорона» поступила в гражданский оборот в пяти городах — Москве, Санкт-Петербурге, Ростове-на-Дону, Туле и Новосибирске. После завершения пострегистрационных клинических испытаний в 2021 году может начаться массовая вакцинация «ЭпиВакКороной»
Вакцина Sinovac Biotech
Фото: Andre Penner / AP
Инактивированная вакцина CoronaVac, разработанная китайской Sinovac Biotech, хранится в холодильнике при плюс 2–8 градусах Цельсия. В Sinovac заявили, что обеспечат производство 300 млн доз в год. Для иммунизации требуется две дозы, а это означает, что CoronaVac смогут привиться 150 млн человек — чуть больше десятой части населения Китая.
Данные об эффективности вакцины от Sinovac разнятся. Последние испытания в Бразилии показали 50,4% эффективности, а в Индонезии и Турции — 65,3% и 91,5% соответственно.
Вакцина была одобрена для экстренного применения в группах высокого риска в Китае с июля. Использование этой вакцины 13 января разрешили власти Турции. Несколько азиатских стран — Сингапур, Малайзия и Филиппины, а также Бразилия и Украина подписали соглашения о закупках CoronaVac
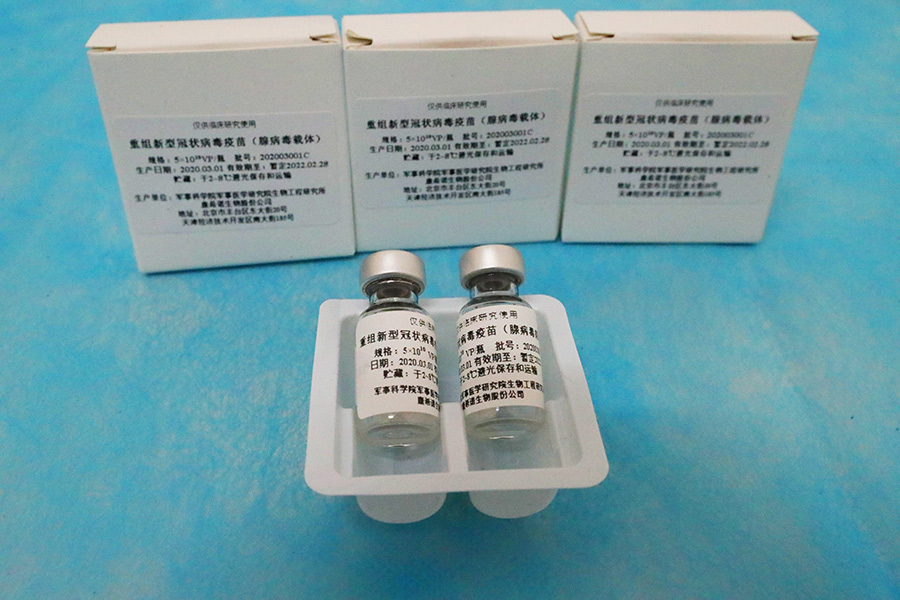
Вакцина CanSino Biologics
Фото: Reuters
Еще одна китайская вакцина Ad5-nCoV («Конвидеция»), на основе человеческого аденовируса типа 5, разработана фармкомпанией CanSino Biologics. Преимуществом этого препарата является однократное введение, а также возможность хранения при температуре от плюс 2 до плюс 8 градусов Цельсия.
В ноябре 2020 года были поданы документы в Минздрав России для регистрации вакцины. В декабре Минздрав выдал разрешение на проведение третьего международного этапа клинического исследования Ad5-nCov. В случае, если вакцина покажет высокую эффективность и безопасность, CanSino Biologics с российским «Петроваксом» организуют ее производство в России.
Согласно промежуточным результатам третьей фазы клинических испытаний в России, Ad5-nCoV показала эффективность в 92,5%. Окончательные результаты исследования появятся в середине 2021 года
Вакцина CNBG (Sinopharm)
Фото: Reuters
Другую китайскую инактивированную вакцину разработала China National Biotec Group (CNBG) (подразделение Sinopharm). Она не требует отрицательной температуры хранения и вводится двумя дозами с интервалом в две недели.
30 декабря Sinopharm объявила, что на третьем этапе испытаний препарат показал эффективность на 79%. Однако Объединенные Арабские Эмираты, которые одобрили вакцину Sinopharm в этом месяце, заявили, что эффективность вакцины составила 86%. Кроме Китая и ОАЭ вакцина Sinopharm проходит клинические испытания в Бахрейне, Иордании, Перу и Аргентине.
В Китае препарат Sinopharm с июля используется в рамках программы по экстренному вакцинированию, а 31 декабря Государственное управление по лекарственным средствам Китая одобрило препарат для широкого использования
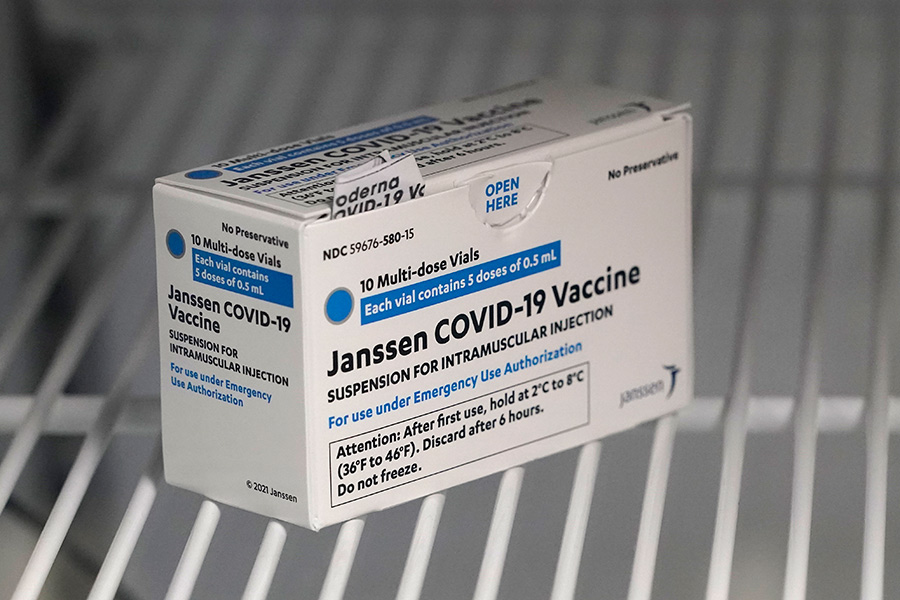
Вакцина Johnson & Johnson
Фото: Ted S. Warren / AP
Вакцину Janssen американской корпорации Johnson & Johnson 11 марта одобрил ЕС. Чуть раньше экстренное применение препарата разрешило Управление США по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA). Препарат также включен в список для экстренного применения ВОЗ.
В ходе клинических испытаний с участием 44 тыс. человек из США, Южной Африки и стран Латинской Америки препарат показал эффективность в 67%.
Вакцина Janssen хранится при температуре -20 градусов по Цельсию. Но у нее есть особенность — на протяжении трех месяцев она может находиться в условиях от 2 до 8 градусов по Цельсию. Главное преимущество — однодозное введение.
Дарья Минько
При участии
Егор Губернаторов
https://ria.ru/20200811/1575637509.html
Разработка вакцин против COVID-19 в мире
Разработка вакцин против COVID-19 в мире — РИА Новости, 11.08.2020
Разработка вакцин против COVID-19 в мире
Всемирная организация здравоохранения (ВОЗ) 31 декабря 2019 года получила уведомление о выявлении в городе Ухань китайской провинции Хубэй кластера случаев… РИА Новости, 11.08.2020
2020-08-11T14:06
2020-08-11T14:06
2020-08-11T14:07
справки
коронавирус covid-19
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdnn21.img.ria.ru/images/07e4/08/0b/1575634109_178:100:1280:720_1920x0_80_0_0_30216a4ea4018aa93269a23dc32358f2.jpg
Всемирная организация здравоохранения (ВОЗ) 31 декабря 2019 года получила уведомление о выявлении в городе Ухань китайской провинции Хубэй кластера случаев заболевания пневмонией неизвестного типа. Седьмого января 2020 года китайские власти установили, что возбудителем данного заболевания является вирус SARS-CoV-2, а 11 февраля 2020 года ВОЗ присвоила ему наименование «коронавирусная инфекция COVID-19», 11 марта 2020 года ВОЗ объявила вспышку COVID-19 пандемией. По данным ВОЗ, число заболевших приближается к 20 миллионам, как минимум 728 тысяч из них погибли. Среди наиболее подверженных вирусу SARS-CoV-2 стран, согласно подсчетам Университета Джонса Хопкинса, – Соединенные Штаты Америки, Бразилия и Индия. Россия остается на четвертой строчке. В рамках реагирования на вспышку ВОЗ активизировала работу Программы научных исследований и разработок (НИОКР), в задачи которой входит ускоренная разработка средств диагностики, вакцин и лекарственных средств, предназначенных для борьбы с новым коронавирусом. По данным ВОЗ на 31 июля 2020 года, 26 вакцин-кандидатов проходили клинические испытания, 139 вакцин находились на стадии доклинических испытаний.В разработках участвуют самые разные организации – от фармацевтических гигантов и крошечных биотехнологических компаний до академических центров и некоммерческих групп. ВОЗ признает, что темпы разработки вакцины от COVID-19 беспрецедентны. Как правило, это дорогостоящий, сложный и длительный процесс, требующий сотен миллионов долларов инвестиций и многих лет испытаний для подтверждения того, что вакцина безопасна и эффективна. Обычно для выпуска новых вакцин на рынок требуется 10-15 лет, сейчас же компании планируют сократить этот срок до года-полутора.Для координации усилий в области разработки вакцин против COVID-19 ВОЗ создала Международную платформу для регистрации клинических испытаний, задача которой состоит в том, чтобы обеспечить всем участвующим в принятии решений доступ к полной картине научных исследований. РоссияРоссия начала разрабатывать вакцину от COVID-19 в январе. В мае вице-премьер РФ Татьяна Голикова сообщала, что в стране ведется разработка 47 вакцин на 14 платформах. В начале июля министр здравоохранения РФ Михаил Мурашко заявил, что 17 вакцин от коронавируса являются перспективными. По словам Голиковой, лидерами по созданию вакцины являются Институт Гамалеи и центр Роспотребнадзора «Вектор». Государственный научный центр «Вектор» разработал прототипы вакцин, основанные на шести различных технологических платформах. Исследователям удалось создать вакцины как на основе широко применяемых рекомбинантных вирусных векторов гриппа, кори и везикулярного стоматита, так и на основе многообещающих технологий синтетических вакцин: мРНК-вакцины, пептидные вакцины и субъединичные вакцины. Для дизайна вакцин использовали современные биоинформационные системы, а конструирование и доведение до готовых прототипов проводили с помощью передовых наработок, в том числе, в области обратной генетики.В середине марта ученые центра «Вектор» начали исследования иммуногенности на чувствительных лабораторных животных всех разработанных прототипов вакцин. Сообщалось, что «Вектор» испытывал вакцины на сирийских хомячках, хорьках, низших приматах вида Macaca mulatta и Chlorocebus aethiops. 14 мая гендиректор научного центра «Вектор» Ринат Максюков сообщил, что лабораторные испытания прототипов вакцины на животных уже завершены и определены три перспективных препарата.Вакцины отличаются не только по своему функциональному началу, но и по способу и схеме иммунизации. По словам Максюкова, один из препаратов, идет не по классической схеме введения внутримышечно, а схема введения интерназальная, то есть фактически он просто закапывается в нос. По словам директора центра «Вектор», животные, на которых испытывали вакцину от коронавируса, хорошо перенесли ее. У некоторых особей отмечалась повышенная температура. Для контроля возможных изменений в легких в «Векторе» использовали рентгеновскую установку. 30 июня гендиректор научного центра «Вектор» Ринат Максюков заявил, что три прототипа вакцины против заболевания COVID-19 успешно прошли испытания на способность формировать иммунный ответ.27 июля в центре «Вектор» с пяти добровольцев начались клинические испытания вакцины «ЭпиВакКорона», в этот день был привит первый доброволец, следующие – с интервалом в 72 часа. Еще через три дня вакцину получат следующие девять человек. На втором этапе клинических исследований вакцины от коронавируса из 86 добровольцев 43 получат плацебо. Новосибирский научный центр «Вектор» планирует начать производство вакцины от коронавируса в ноябре. В середине февраля в гонку по созданию вакцины против COVID-19 включились ученые Национального исследовательского центра эпидемиологии и микробиологии имени Н.Ф. Гамалеи. 16 мая стало известно, что в НИЦ Гамалеи создали вакцину, позволяющую выработать антитела и защиту для организма. На тот момент сотрудники центра проводили официальные доклинические испытания, где определяется токсичность, реактогенность и прочие свойства вакцины. Сотрудники, которые занимаются непосредственно разработкой вакцины, сделали себе прививку еще 30 марта. Глава НИЦ Гамалеи Александр Гинцбург призвал не расценивать это как испытания, отметив, что самозащита была необходима для продолжения дальнейшей работы без рисков ухода на самоизоляцию. 25 мая стало известно, что у всех сотрудников, сделавших себе прививку, обнаружены протективные антитела (вируснейтрализующие). Позднее стало известно, что успешные испытания вакцины на токсичность, безопасность, иммуногенность и защитную эффективность на крупных и мелких животных были проведены в 48 Центральном научно-исследовательском институте Минобороны России. По словам Гинцбурга, вакцина от коронавируса будет действовать более двух лет. Препарат использует аденовирусные контейнеры для доставки генов, кодирующих белок «короны» у вируса. Его будут вводить два раза. Как пояснил ученый, один и тот же ген вводится на разных носителях – это дает возможность получить защитный протективный иммунитет, причем на увеличенный период времени.По словам Александра Гинцбурга, такой подход гарантирует с большой вероятностью, что человек, получивший эту вакцину в бустерном, то есть усиливающем варианте, будет защищен от возможного заражения коронавирусом, «по крайней мере, в течение двух лет, а возможно, и на более длительный период».Гинцбург также уточнил, что такое длительное действие препарата удалось доказать при совместной работе НИЦ и медицинских учреждений российского Минобороны в африканской Гвинее над вакцинами против вируса Эбола. 16 июня Минздрав России выдал разрешение на проведение клинических исследований двух форм вакцины против новой коронавирусной инфекции COVID-19, разработанной ФГБУ НИЦ эпидемиологии и микробиологии им. Н.Ф. Гамалеи Минздрава России. Исследования двух форм вакцины (в форме раствора для внутримышечного введения и в виде порошка для приготовления раствора для внутримышечного введения; рабочие названия вакцин – «Гам-КОВИД-Вак» и «Гам-КОВИД-Вак Лио») проводились с 18 июня в военном госпитале им. Бурденко и в Сеченовском университете. До начала клинических испытаний добровольцев подробно обследовали, в том числе проверили на отсутствие антител к коронавирусу. Затем их на две недели изолировали, чтобы не допустить инфицирования. Добровольцев разделили на две группы – участники первой получили одну дозу вакцины, второй – две. Вакцинация проходила в два этапа – в нулевой день и на 21-й, после вакцинации добровольцы находились в изоляции в стационаре 28 дней, где врачи контролировали их состояние. Также врачи будут контролировать состояние здоровья добровольцев в течение шести месяцев после выписки из стационара. Директор Института медицинской паразитологии, тропических и трансмиссивных заболеваний Сеченовского университета Александр Лукашев 12 июля сообщил, что безопасность вакцины подтверждена в ходе клинических испытаний. По словам Лукашева, инъекция не вызвала негативной реакции организма, за исключением повышения температуры тела в первые дни после вакцинации. Вторая фаза испытаний вакцины завершена; третья фаза будет проходить не только в России, но и за рубежом. 11 августа президент РФ Владимир Путин объявил о регистрации в России первой вакцины от коронавируса. Производить препарат планируют на двух площадках: в самом Центре Гамалеи и в компании «Биннофарм». Согласно данным государственного реестра лекарственных средств Минздрава, российская вакцина поступит в гражданский оборот 1 января 2021 года.В Санкт-Петербургском научно-исследовательском институте вакцин и сывороток ФМБА России создали препарат на основе рекомбинантного белка и наночастиц. Клинические испытания вакцины планируется начать в сентябре-декабре, а в октябре-декабре предоставить регистрационное досье и выйти на промышленное производство в декабре. Биотехнологическая компания из Санкт-Петербурга Biocad работает над тремя вакцинами от COVID-19. Одну из вакцин на основе везикулярного стоматита Biocad разрабатывает совместно с Государственным научным центром «Вектор». Согласно соглашению, Biocad берет на себя расходы и организационные усилия, связанные с проведением клинических исследований rVSV-вакцины, созданием технологии выпуска препарата и самим производством. Над второй вакциной, на основе аттенуированной (ослабленной) основы вируса гриппа, Biocad работает совместно с Институтом экспериментальной медицины в Санкт-Петербурге. На основе собственных наработок по онковакцинам Biocad разрабатывает инкапсулированную в липосомы мРНК-вакцину против COVID-19.Федеральный научный центр исследований и разработки иммунобиологических препаратов им. М.П. Чумакова работает над созданием цельновирионной инактивированной (с искусственно ослабленными вирусами) вакцины. Центр успешно завершил доклинические испытания. По словам генерального директора Федерального научного центра исследований и разработки иммунобиологических препаратов им. М.П. Чумакова Айдара Ишмухаметова, в испытаниях принимали участие не только мелкие грызуны, но и приматы, чья реакция на вакцинацию максимально приближена к человеческой. Испытания показали высокую эффективность и безопасность вакцины. Центр имени Чумакова планирует приступить к испытаниям вакцины против COVID-19 в конце августа. В испытаниях примут участие более 100 добровольцев. Ученые Казанского федерального университета (КФУ) разрабатывают вакцину на основе опубликованного генома вируса с помощью генной инженерии. Профессор кафедры генетики Института фундаментальной медицины и биологии КФУ Альберт Ризванов уточнял, что ученые не могут работать с живым вирусом, поскольку для этого необходима лаборатории высокого уровня биологической безопасности. Ученые могут создать искусственную молекулу ДНК, которая содержит часть вирусного генома. Если такую ДНК-вакцину ввести в организм, то он считает генетическую информацию. Организм начинает синтезировать отдельные вирусные белки, иммунная система распознает их как чужеродные, и вырабатывается защитный ответ. По словам Ризванова, это уникальный подход: ученые КФУ единственные в мире, кто использует комбинацию вирусных генов при создании ДНК-вакцины. 23 июня стало известно, что Казанский федеральный университет приступил к тестированию вакцины против нового коронавируса на лабораторных животных. 24 июля сообщалось, что первый этап апробации вакцины оказался результативным.На втором этапе исследователи анализируют итоги проведения повторной иммунизации. По словам Альберта Ризванова, параллельно с подведением итогов и подтверждением результатов второй иммунизации ученые продолжают работать над второй версией вакцины. Известно, что на базе биологического факультета МГУ имени М.В. Ломоносова под руководством академика Михаила Кирпичникова разрабатывается прототип поливалентной вакцины против COVID-19, то есть такой, которая бы работала в отношении широкого спектра коронавирусов. Биологи МГУ на основе вирусов растений создали несколько прототипов поливалентной вакцины против коронавирусов, вызывающих такие заболевания как COVID-19, SARS, MERS и коронавирусов летучих мышей, имеющих потенциал преодоления межвидового барьера с человеком. В Институте биоорганической химии имени Шемякина и Овчинникова под руководством академика Александра Габибова разрабатывается «современная высокотехнологичная вакцина против COVID-19 на основе вирусоподобных частиц с использованием так называемых рекомбинантных фрагментов белков коронавируса». Сообщалось, что в июле-октябре планируется провести доклинические испытания опытных образцов на мышах. В Институте общей генетики имени Вавилова разрабатывается вакцина, которая несет на своей поверхности три белка коронавируса, что поможет создать также поливалентную вакцину. Работы идут под руководством профессора Козлова, крупнейшего специалиста в области ДНК-вакцин. В Институте экспериментальной медицины в Санкт-Петербурге разрабатывают «мукозальную вакцину против SARS-CoV-2». Ее разработчики методами генной инженерии встроили в ворсинки на поверхности микробов-пробиотиков S-белок – ключевую молекулу, благодаря которой коронавирус SARS-CoV-2 проникает в клетки. В результате формируется бактерия с иммуногенным белком вируса на поверхности. Вакцину можно будет вводить в организм в виде кисломолочного продукта. В начале июня проводились доклинические испытания этой вакцины. НИИ гриппа имени А.А. Смородинцева Минздрава России сообщал о наборе добровольцев для испытания вакцины от COVID-19. В сообщении института сказано, что вакцина прошла испытания I и II фазы в Китае. Были привиты 500 добровольцев, доказана ее безопасность и эффективность. Идет набор добровольцев в клиническое исследование вакцины (III фаза). Планируемое начало – середина августа. В конце июня стало известно, что в Санкт-Петербургском Политехническом Университете Петра Великого (СПбПУ) начали разработку вакцины от коронавируса на основе самореплицирующейся РНК. Крымский федеральный университет имени В.И. Вернадского начал разрабатывать в начале июля вакцину против нового коронавируса с использованием конструкций на основе тиофосфатных олигонуклеотидов. Ученые пытаются разработать и успешно применить олигонуклеотидную конструкцию в форме «лассо», которая способна одновременно активизировать как клеточный, так и гуморальный иммунитет. Отмечается, что исследователи университета подали заявку на грант Российского фонда фундаментальных исследований на разработку вакцины. КитайПосле того как в Китае произошла вспышка коронавируса, необходимо было как можно скорее приступить к разработке вакцины, местные ученые и профильные компании не стали концентрироваться только на одном виде вакцин, а начали исследовать сразу пять: рекомбинантная субъединичная вакцина, инактивированная вакцина, вакцина на основе аденовирусного вектора, вакцина на основе нуклеиновых кислот и живая аттенуированная гриппозная вакцина. Первую одобренную для испытаний вакцину разработала исследовательская группа во главе с академиком Военно-медицинской академии КНР Чэнь Вэй. Сообщалось также, что одобрение на клинические испытания инактивированной вакцины получила команда Уханьского института вирусологии при Китайской академии наук и Уханьского института биопрепаратов (входит в состав Sinopharm Group), а также пекинская компания Sinovac Research & Development Co. 15 мая стало известно, что китайские ученые испытали пять различных вакцин от коронавирусной инфекции COVID-19 на более чем 2500 добровольцев. В том числе на первой стадии клинические испытания были проведены на 539 добровольцах, имелись данные о безопасности и выработке антител у испытуемых. На второй стадии испытания вакцины прививки были сделаны 2036 добровольцам. При проведении этих клинических испытаний не получено сообщений о побочных эффектах. Третья фаза клинических испытаний вакцины компании Sinovac пройдет в Бразилии, Индонезии, Бангладеш. 19 июня Государственное управление по надзору за пищевыми продуктами и лекарственными средствами одобрило проведение клинических испытаний рекомбинантной вакцины от COVID-19, разработанной совместно компанией Zhifei Long Kema (дочернее предприятие Chongqing Zhifei Biological Products) и институтом микробиологии Китайской академии наук. Всемирная организация здравоохранения в апреле заявляла, что ближе всех к завершению находится вакцина, разработанная компанией CanSino Biologics Inc. в Гонконге и Пекинским институтом биотехнологии. 25 июня рекомбинантная вакцина от COVID-19 (на основе аденовирусного вектора) Ad5-nCoV, совместно разработанная CanSino Biologics, Пекинским институтом биотехнологий и Академией военно-медицинских наук Народно-освободительной армии Китая, получила специальное разрешение сроком на один год от управления по вопросам гигиены и здравоохранения объединенных сил материально-технического обеспечения при Центральном военном совете (ЦВС) КНР.Сообщалось, что первая и вторая фазы клинических тестов указанной вакцины прошли на территории Китая, полученные в результате испытаний данные показали хороший уровень безопасности и высокий уровень гуморального и клеточного иммунного ответа.В компании подчеркнули, что вакцина Ad5-nCoV в настоящий момент ограничена лишь военным использованием, для более широкого применения необходимо будет отдельное разрешение соответствующего департамента ЦВС КНР. В конце июня началась первая фаза клинических испытаний китайской РНК-вакцины, которую разрабатывают Академия военно-медицинских наук КНР, Suzhou Abogen Biosciences и Walvax Biotechnology Co. В них участвуют 168 волонтеров, одна возрастная группа – от 18 до 59 лет, другая – от 60 лет. Сообщалось, что пациентам введут по две дозы вакцины в амбулаторном режиме. СШААдминистрация США запустила в мае операцию Warp Speed – совместный проект министерства здравоохранения и Пентагона, целью которого является производство 300 миллионов доз вакцины от COVID-19 к январю 2021 года.Несколько вакцин, разрабатываемых американскими компаниями, считаются перспективными. В середине марта Национальный институт аллергии и инфекционных заболеваний в Сиэтле (штат Вашингтон) объявил о начале клинических испытаний на людях вакцины от нового коронавируса SARS-CoV-2. Вакцина, получившая название мРНК-1273, разработана Национальным институтом аллергии и инфекционных заболеваний США (NIAID) совместно с биотехнологической компанией Moderna, базирующейся в Кембридже, штат Массачусетс. Вакцина мРНК-1273 была разработана с использованием генетической платформы, называемой мРНК (мессенджер РНК). Она направляет клетки организма на экспрессию вирусного белка, который, как надеются ученые, вызовет сильный иммунный ответ. Вакцина успешно прошла испытания на животных.Исследователи надеются, что с ее помощью им удастся настроить иммунную систему человека для борьбы с вирусом. Для испытания отобрали 45 добровольцев, которым планировалось вводить по две инъекции вакцины с интервалом в 28 дней. Сами дозы у участников эксперимента должны были различаться: 25, 100 и 150 микрограммов. Исследование должно было оценить вакцину на безопасность и способность вызывать иммунный ответ, а также определить оптимальную дозировку. 18 мая компания Moderna объявила о позитивном завершении первой фазы клинических испытаний вакцины от коронавируса. В заявлении Moderna отмечается, что после приема вакцины mRNA-1273 количество антител участников испытаний в зависимости от дозы препарата или превышало соответствующий показатель в крови людей, переболевших COVID-19, или находилось на том же уровне. На начальной стадии препарат показал себя безопасным, он переносится без осложнений. C 27 июля Moderna приступила к испытаниям вакцины, в которых участвуют около 30 тысяч добровольцев.Каждый получает дозу потенциальной вакцины в размере 0,1 миллиграмма, через 29 дней инъекция повторяется. Некоторые участники будут привиты препаратом-плацебо. В июне Moderna опубликовала данные предварительного исследования от COVID-19 на мышах. Сообщалось, что ученые ввели различные количества вакцины шестинедельным мышам, включая дозы, считающиеся недостаточно сильными, чтобы вызвать защитный иммунный ответ. Затем исследователи подвергли мышей воздействию вируса.Как подчеркивают ученые, полученные предварительные данные показали, что вакцина является «мощным иммуногенным веществом» и нейтрализующая активность «может быть достигнута с помощью одной дозы». Кроме того, отмечается, что «субпротективные дозы не приводили к усиленной иммунопатологии» после воздействия вируса у мышей, то есть не вызывали более тяжелого течения болезни.Дальнейшее тестирование показало, что вакцина вызывает мощный ответ нейтрализующих антител. Это то, что необходимо для блокирования вируса, чтобы он не поражал клетки. Вакцина также защищает легкие от заражения коронавирусом без признаков токсического воздействия. В начале апреля сообщалось, что специалисты Питтсбургского университета в США разработали вакцину от коронавируса и успешно испытали ее на мышах. К тестированию на людях они надеются приступить в ближайшие месяцы. Вакцина получила название PittCoVacc (сокращение от Pittsburgh Coronavirus Vaccine). Вакцина на основе вирусного антигена доставляется в кожу с помощью микроигл, расположенных на поверхности пластыря размером с кончик пальца. Микроигольный пластырь, внешне похожий на «липучку», содержит 400 крошечных микроигл из сахаров и белков, которые полностью растворяются, не оставляя следов. Результаты исследования на мышах показали, что при такой форме подачи вакцины у животных через две недели вырабатывались антитела, специфичные к SARS-CoV-2, в количествах, которые считаются достаточными для нейтрализации вируса. По словам исследователей, такие пластыри могут быть быстро изготовлены в промышленных масштабах, и их не нужно держать в холоде во время хранения или транспортировки. Это большое преимущество перед традиционной формой вакцины. В середине мая американская биотехнологическая компания Inovio сообщила о позитивных результатах ее вакцины против COVID-19 в рамках доклинических испытаний, ДНК-вакцина INO-4800 демонстрирует активное реагирование нейтрализующих антител и Т-лимфоцитов на коронавирус SARS-CoV-2.Вакцина INO-4800 нацелена против главного поверхностного шиповидного белка вируса SARS-CoV-2, из-за которого возникает COVID-19. В рамках исследования было выявлено, что вакцинирование INO-4800 создавало у мышей и морских свинок, на которых проводились испытания, стойкие антитела и Т-лимфоциты, которые реагировали на коронавирус.В конце июня компания Inovio сообщала об успешном испытании вакцины на обезьянах. В компании сообщили, что эти результаты доклинических испытаний, а также иммунное реагирование на начальных стадиях клинических испытаний могут позволить уже летом перейти ко второй фазе испытаний. Фармацевтическая компания Novavax в мае начала первые клинические испытания на людях разработанной ею вакцины от коронавируса. Наночастичковая вакцина, представляющая S-белок SARS-CoV-2 с сапониновым адъювантом получена с использованием запатентованной технологии наночастиц. Вакцина включает в себя адъювант Matrix‑M™ для усиления иммунных реакций и стимуляции высоких уровней нейтрализующих антител. 4 августа Novavax сообщила о двух успешных исследованиях потенциальной вакцины от коронавируса, которую она производит. В одном из исследований 56 волонтеров показали высокий уровень антител на вирус без опасных побочных эффектов. Во втором исследователи обнаружили, что вакцина защищает подопытных приматов от заражения коронавирусом. Компания Janssen (является структурным подразделением Johnson & Johnson) разрабатывает рекомбинантную вакцину против SARS-CoV-2 – Ad26.COV2-S. В июле было объявлено об успехе доклинических испытаний. В США и Бельгии начались клинические испытания вакцины. Группа добровольцев состоит из 1045 здоровых людей в возрасте от 18 до 55 лет и взрослых в возрасте от 65 лет и старше.СингапурСингапурская медицинская школа Duke-NUS совместно с расположенной в США Arcturus Therapeutics (компания по производству РНК-препаратов) разрабатывают вакцину LUNAR-COV19, которая основана на самореплицирующейся мРНК. Данные доклинических исследований показали, что уровни нейтрализующих антител в ответ на однократную дозу LUNAR-COV19 продолжают расти в течение 50 дней. 21 июля было объявлено о переходе к клиническим испытаниям. ТаиландТайская группа исследователей под руководством Киата Ракрунгтхама из Центра разработки вакцин Чулалонгкорнского университета в сотрудничестве с университетом Пенсильвании (США) работает над вакциной CU-Cov19. 12 июля ученые завершили тесты на обезьянах и объявили о готовности приступить к тестам на людях-добровольцах в октябре, затем последует вторая фаза испытаний – с декабря по март 2021 года. Третья фаза испытаний на людях требует более 10 тысяч участников, чтобы признать результаты действительными. В связи с относительно небольшим количеством случаев в Таиланде, для проведения третьей фазы испытаний предполагается сотрудничество с Бразилией, Индией и Индонезией. Ученые используют новую технологию, основанную на мРНК. ИндияВ Индии, которая считается одним из крупнейших производителей лекарств в мире, разработкой препарата против COVID-19 занимается несколько компаний. Одна из них – биотерапевтическая компания Bharat Biotech, на счету которой 16 успешно используемых вакцин, в том числе против свиного гриппа (H1N1). Совместно с индийским Советом медицинских исследований и Национальным институтом вирусологии компания разработала вакцину под названием Covaxin.Вакцина разработана на основе штамма вируса, который был выделен локально и ослаблен в лабораторных условиях. В начале июля компания Bharat Biotech получила одобрение управления генерального контролера лекарств Индии на клинические испытания разработанного препарата Covaxin на людях. Вместе с вирусологами из Висконсинского университета в Мадисоне и компанией FluGen, компания Bharat Biotech разрабатывает препарат под названием CoroFlu. По словам представителей компаний-разработчиков, его основу будет составлять экспериментальная вакцина против гриппа от FluGen. В отличие от многих других вакцин, CoroFlu предполагается вводить интраназально, то есть внутрь носа, так как этот способ имитирует естественное попадание инфекции. Кроме того, этот способ введения препарата, как говорят в компании-разработчике, более эффективен и вызывает более сильный иммунный ответ.В начале июля стало известно, что вторая индийская фирма начала клинические испытания вакцины от коронавируса на людях после получения одобрения от управления генерального контролера лекарств Индии. Препарат разработала компания Zydus Cadila Healthcare Ltd. 5 августа было объявлено о безопасности вакцины. С 6 августа начались испытания этой вакцины на более, чем тысячи добровольцев. Также в разработку вакцин включились Институт сыворотки Индии (совместно с американской Codagenix), компания Panacea Biotec (совместно с американской Refana), биофармацевтическая компания Indian Immunologicals (совместно с австралийским университетом Гриффита). ЯпонияВ марте японская фармацевтическая компания «Энджес» (AnGes) объявила о совместной разработке ДНК-вакцины против нового коронавируса COVID-19 с Университетом города Осака. Компания «Энджес» специализируется на разработке ДНК-плазмида HGF, внехромосомного самовоспроизводящегося генетического элемента, и с помощью этой технологии будет создаваться вакцина от коронавируса. 30 июня компания AnGes, Inc приступила к клиническим испытаниям на двух группах из 30 добровольцев. Учредитель компании, ее советник по медицинским вопросам, профессор департамента клинической генотерапии университета Осака Рюити Морисита рассказал, что добровольцы разделены на две группы. Одной группе планировалось вводить меньшее количество вакцины, другой – большее. Вакцинирование планировалось проводить дважды с интервалом в две недели.Вторая часть исследований с участием 400-500 человек намечена на осень, а к весне AnGes, Inc. рассчитывает выйти на этап промышленного производства вакцины. Главными преимуществами ДНК-вакцины профессор Морисита считает ее безопасность – она не использует патогены, организм создает антитела, реагируя не на патоген, а на ДНК-информацию о нем. Также он отметил возможность произвести вакцину быстро и фактически в неограниченном количестве. Достоинством вакцины ученый считает и то обстоятельство, что ее производство можно гибко подстроить под новые мутации вируса, если таковые произойдут. Южная Корея / Австралия12 мая австралийский разработчик вакцин Vaxine Pty заключил соглашение с южнокорейской компанией Medytox о совместной разработке вакцины COVAX-19 от нового коронавируса. 2 июля стало известно, что первые клинические испытания вакцины начались в клиническом исследовательском центре PARC Royal Adelaide Hospital. Сообщалось, что в ходе первой части исследования 40 предварительно отобранным кандидатам в возрасте от 18 до 65 лет будут назначены две дозы вакцины или плацебо с интервалом в три недели. Выработка антител и другие иммунные реакции должны быть проанализированы через две недели после второй инъекции, а данные, как ожидается, будут доступны примерно через два месяца. Разработкой вакцины от коронавируса также занимается Университет Квинсленда (Австралия) совместно с биотехнологической компанией CSL. Вакцина уже проходит первую фазу клинических испытаний. В них участвуют 120 здоровых добровольцев. 11 июня вакцина от COVID-19, разрабатываемая южнокорейской компанией Genexine Consortium, получила одобрение на проведение клинических испытаний. Разработка представляет собой ДНК-вакцину. Сообщалось, что исследование будет состоять из первой фазы с участием 40 здоровых добровольцев, за которой последует плацебо-контролируемая фаза IIa оценки двух уровней дозы для обеспечения безопасности и эффективности у 150 пациентов. Ожидалось, что первый этап будет завершен в течение трех месяцев, за которым во второй половине 2020 года последует второй. Данная фаза исследований будет проводиться в нескольких странах. КанадаКанадская биофармацевтическая компания Medicago, штаб-квартира которой находится в Квебеке, работает над вакциной, основанной на так называемом S-белке, присутствующем на поверхности коронавируса. 14 июля Medicago сообщила, что начинает первую стадию клинических испытаний, которая заключается в случайном наблюдении за 180 здоровыми добровольцами, мужчинами и женщинами в возрасте от 18 до 55 лет. В ходе проверки вакцины будет оценена приемлемая дозировка самой вакцины на растительной основе и в комбинации с вспомогательным стимулирующим веществом.Вторую стадию клинических испытаний растительной вакцины Medicago планируется начать в октябре. Ожидается, что вакцина будет доступна в 2021 году. ЕвропаБиотехнологические компании ReiThera (Италия), Leukocare (Германия) и Univercells (Бельгия) создали консорциум, чтобы ускорить разработку и массовое производство препарата против COVID-19. Вакцина, над которой работают компании, будет создана на основе аденовирусных векторов. Ожидается, что 24 августа 2020 года начнутся испытания вакцины на добровольцах. Испытания будет проводить Национальный институт инфекционных заболеваний Lazzaro Spallanzani в Риме, в них примут участие 90 добровольцев. Если клинические испытания будут успешны, компании в этом году намерены приступить к производству препарата. Согласно планам консорциума, в начале 2021 года планируется произвести около 6 миллионов доз.Как заявила представитель компании Leukocare Ева Бауэр, данные, полученные в результате клинических исследований, показывают, что аденовирусные векторы безопасны и «вызывают устойчивой иммунный ответ от одной дозы».Вакцина против COVID-19, разработанная исследователями из Копенгагенского университета, работающих в рамках европейского консорциума Prevent-Ncov Consortium, была протестирована на мышах. Используемая исследователями технология называется cVLP, что означает «капсидная вирусоподобная частица» (capsid Virus-Like Particle). После введения вакцины мыши производили большое количество антител, способных нейтрализовать вирус SARS-CoV-2. Количество и качество этих антител, индуцированных вакциной, были протестированы непосредственно на вирусе SARS-CoV-2 в двух независимых лабораториях Орхусского университета и медицинском центре Лейденского университета. Исследователи надеются начать клинические испытания до конца года. ГерманияНемецкая фармацевтическая компания CureVac летом начала исследование первой фазы вакцины от COVID-19. Сообщалось, что вакцину планируется ввести 168 добровольцам в Тюбингене, Мюнхене, Ганновере и бельгийском городе Генте. Компания планирует выйти на следующую фазу исследования осенью. Если тестирование будет успешным, CureVac начнет более масштабные клинические испытания при участии нескольких тысяч человек.Финансирование данных работ на сумму в более чем 80 миллионов евро намерен поддержать ЕС.Компания CureVac существует с 2000 года, она была создана на базе университета Тюбингена. Ранее власти ФРГ жестко отреагировали на попытку администрации США выкупить права на новую вакцину против коронавируса, разработкой которой занимается CureVac. В конце апреля Институт вакцины и биомедицинских препаратов имени Пауля Эрлиха одобрил первое клиническое испытание вакцины против COVID-19, разработанном биоинженеринговой компанией BioNTech из немецкого города Майнц. Кроме того, BioNTech совместно с фармацевтической компанией Pfizer начала клинические испытания в США – с участием около 8000 человек. Также запланированы клинические испытания вакцины на 30 000 добровольцах. В настоящее время в США и Германии проходит первая и вторая фаза клинических испытаний в общей сложности четырех версий вакцины BNT 162. В июле Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило ускоренную процедуру утверждения двух версий вакцины (BNT162b1 и BNT162b2). ФранцияНациональный институт здравоохранения и медицинских исследований Франции Inserm при поддержке ряда государственных профильных институтов и организаций создает единую платформу вакцин-кандидатов против COVID-19 для проведения их крупномасштабной клинической качественной оценки. Платформа получила название COVIREIVAC. Транснациональный фармацевтический гигант Sanofi работает над двумя проектами вакцины от коронавируса, один из них – в партнерстве с британским фармацевтическим гигантом GlaxoSmithKline (GSK) и при поддержке связанного с американским Минздравом агентства BARDA, которое уже выделило Sanofi около 30 миллионов долларов. Вакцина основана на технологии рекомбинации ДНК, которая уже применяется при создании антигриппозных вакцин. Начать клинические испытания планируется в сентябре этого года. Одновременно Sanofi ведет разработку и другой вакцины от коронавируса в сотрудничестве с биотехнологической компанией Translate Bio. Данная вакцина создается методом переноса фрагмента РНК, генетического кода вируса. По этой вакцине клинические испытания первой фазы запланированы на период до конца года. Институт Пастера совместно с группой MSD и компанией Themis Bioscience разрабатывают вакцину на основе аттенуированного штамма кори, который был генетически модифицирован. В конце июня научный руководитель Института Кристоф д`Анфер сообщил, что группа готовится в течение июля начать тестирование на 90 добровольцах во Франции и Бельгии. Организация 2-й и 3-й фаз испытаний планируется совместно с Питтсбургским университетом. ВеликобританияВ мае компания AstraZeneca заключила партнерство с Оксфордским университетом для разработки, производства и поставки вакцины от COVID-19. Вакцина ChAdOx1 nCoV-19, разработанная Институтом Дженнера Оксфордского университета совместно с Оксфордской группой по изучению вакцин, использует вирусный вектор на основе ослабленной версии обычной простуды (аденовирус), который содержит генетический материал шиповидного белка SARS-CoV-2. После вакцинации происходит синтез поверхностного шиповидного белка, что приводит к формированию иммунного ответа на COVID-19 при возможном последующем заражении эти вирусом. В конце мая ученые приступили к третьей фазе клинических испытаний вакцины. 17 июля было объявлено, что в том случае, если разработка AstraZeneca и Оксфордского университета окажется удачной, российская компания «Р-Фарм» возьмет на себя часть производства для поставок на российский рынок и многие другие страны. Также известно, что вакцину от коронавируса разрабатывают в лондонском университете Imperial College, она может быть готова для применения в первой половине 2021 года. Разработку финансирует правительство Великобритании.Препарат производится синтетическим путем. По словам одного из разработчиков, профессора Робина Шаттока, после внутримышечной инъекции препарат усиливает РНК и стимулирует иммунный ответ организма на инфекцию. В конце июня начались испытания вакцины на добровольцах. 17 июля началась вторая фаза клинических испытаний. Биотехнологическая фирма Kentucky BioProcessing, принадлежащая табачной компании British American Tobacco (BAT), работает над созданием вакцины с использованием растений табака. На стадии доклинических испытаний препарат дал положительный иммунный ответ. Ожидается, что клинические испытания вакцины начнутся 14 сентября 2020 года. Материал подготовлен на основе информации РИА Новости и открытых источников
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
2020
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
https://cdnn21.img.ria.ru/images/07e4/08/0b/1575634109_320:0:1280:720_1920x0_80_0_0_c30b721b65ee51735b92f1885a967faa.jpg
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
справки, коронавирус covid-19
Справки, Коронавирус COVID-19
Всемирная организация здравоохранения (ВОЗ) 31 декабря 2019 года получила уведомление о выявлении в городе Ухань китайской провинции Хубэй кластера случаев заболевания пневмонией неизвестного типа. Седьмого января 2020 года китайские власти установили, что возбудителем данного заболевания является вирус SARS-CoV-2, а 11 февраля 2020 года ВОЗ присвоила ему наименование «коронавирусная инфекция COVID-19», 11 марта 2020 года ВОЗ объявила вспышку COVID-19 пандемией. По данным ВОЗ, число заболевших приближается к 20 миллионам, как минимум 728 тысяч из них погибли. Среди наиболее подверженных вирусу SARS-CoV-2 стран, согласно подсчетам Университета Джонса Хопкинса, – Соединенные Штаты Америки, Бразилия и Индия. Россия остается на четвертой строчке.
В рамках реагирования на вспышку ВОЗ активизировала работу Программы научных исследований и разработок (НИОКР), в задачи которой входит ускоренная разработка средств диагностики, вакцин и лекарственных средств, предназначенных для борьбы с новым коронавирусом.
По данным ВОЗ на 31 июля 2020 года, 26 вакцин-кандидатов проходили клинические испытания, 139 вакцин находились на стадии доклинических испытаний.
В разработках участвуют самые разные организации – от фармацевтических гигантов и крошечных биотехнологических компаний до академических центров и некоммерческих групп.
ВОЗ признает, что темпы разработки вакцины от COVID-19 беспрецедентны. Как правило, это дорогостоящий, сложный и длительный процесс, требующий сотен миллионов долларов инвестиций и многих лет испытаний для подтверждения того, что вакцина безопасна и эффективна. Обычно для выпуска новых вакцин на рынок требуется 10-15 лет, сейчас же компании планируют сократить этот срок до года-полутора.
Для координации усилий в области разработки вакцин против COVID-19 ВОЗ создала Международную платформу для регистрации клинических испытаний, задача которой состоит в том, чтобы обеспечить всем участвующим в принятии решений доступ к полной картине научных исследований.
Россия
Россия начала разрабатывать вакцину от COVID-19 в январе. В мае вице-премьер РФ Татьяна Голикова сообщала, что в стране ведется разработка 47 вакцин на 14 платформах. В начале июля министр здравоохранения РФ Михаил Мурашко заявил, что 17 вакцин от коронавируса являются перспективными.
По словам Голиковой, лидерами по созданию вакцины являются Институт Гамалеи и центр Роспотребнадзора «Вектор».
Государственный научный центр «Вектор» разработал прототипы вакцин, основанные на шести различных технологических платформах. Исследователям удалось создать вакцины как на основе широко применяемых рекомбинантных вирусных векторов гриппа, кори и везикулярного стоматита, так и на основе многообещающих технологий синтетических вакцин: мРНК-вакцины, пептидные вакцины и субъединичные вакцины. Для дизайна вакцин использовали современные биоинформационные системы, а конструирование и доведение до готовых прототипов проводили с помощью передовых наработок, в том числе, в области обратной генетики.
В середине марта ученые центра «Вектор» начали исследования иммуногенности на чувствительных лабораторных животных всех разработанных прототипов вакцин.
Сообщалось, что «Вектор» испытывал вакцины на сирийских хомячках, хорьках, низших приматах вида Macaca mulatta и Chlorocebus aethiops. 14 мая гендиректор научного центра «Вектор» Ринат Максюков сообщил, что лабораторные испытания прототипов вакцины на животных уже завершены и определены три перспективных препарата.
Вакцины отличаются не только по своему функциональному началу, но и по способу и схеме иммунизации. По словам Максюкова, один из препаратов, идет не по классической схеме введения внутримышечно, а схема введения интерназальная, то есть фактически он просто закапывается в нос.
По словам директора центра «Вектор», животные, на которых испытывали вакцину от коронавируса, хорошо перенесли ее. У некоторых особей отмечалась повышенная температура.
Для контроля возможных изменений в легких в «Векторе» использовали рентгеновскую установку. 30 июня гендиректор научного центра «Вектор» Ринат Максюков заявил, что три прототипа вакцины против заболевания COVID-19 успешно прошли испытания на способность формировать иммунный ответ.
27 июля в центре «Вектор» с пяти добровольцев начались клинические испытания вакцины «ЭпиВакКорона», в этот день был привит первый доброволец, следующие – с интервалом в 72 часа. Еще через три дня вакцину получат следующие девять человек. На втором этапе клинических исследований вакцины от коронавируса из 86 добровольцев 43 получат плацебо. Новосибирский научный центр «Вектор» планирует начать производство вакцины от коронавируса в ноябре.
В середине февраля в гонку по созданию вакцины против COVID-19 включились ученые Национального исследовательского центра эпидемиологии и микробиологии имени Н.Ф. Гамалеи. 16 мая стало известно, что в НИЦ Гамалеи создали вакцину, позволяющую выработать антитела и защиту для организма. На тот момент сотрудники центра проводили официальные доклинические испытания, где определяется токсичность, реактогенность и прочие свойства вакцины.
Сотрудники, которые занимаются непосредственно разработкой вакцины, сделали себе прививку еще 30 марта. Глава НИЦ Гамалеи Александр Гинцбург призвал не расценивать это как испытания, отметив, что самозащита была необходима для продолжения дальнейшей работы без рисков ухода на самоизоляцию. 25 мая стало известно, что у всех сотрудников, сделавших себе прививку, обнаружены протективные антитела (вируснейтрализующие).
Позднее стало известно, что успешные испытания вакцины на токсичность, безопасность, иммуногенность и защитную эффективность на крупных и мелких животных были проведены в 48 Центральном научно-исследовательском институте Минобороны России.
По словам Гинцбурга, вакцина от коронавируса будет действовать более двух лет. Препарат использует аденовирусные контейнеры для доставки генов, кодирующих белок «короны» у вируса. Его будут вводить два раза. Как пояснил ученый, один и тот же ген вводится на разных носителях – это дает возможность получить защитный протективный иммунитет, причем на увеличенный период времени.
По словам Александра Гинцбурга, такой подход гарантирует с большой вероятностью, что человек, получивший эту вакцину в бустерном, то есть усиливающем варианте, будет защищен от возможного заражения коронавирусом, «по крайней мере, в течение двух лет, а возможно, и на более длительный период».
Гинцбург также уточнил, что такое длительное действие препарата удалось доказать при совместной работе НИЦ и медицинских учреждений российского Минобороны в африканской Гвинее над вакцинами против вируса Эбола.
16 июня Минздрав России выдал разрешение на проведение клинических исследований двух форм вакцины против новой коронавирусной инфекции COVID-19, разработанной ФГБУ НИЦ эпидемиологии и микробиологии им. Н.Ф. Гамалеи Минздрава России. Исследования двух форм вакцины (в форме раствора для внутримышечного введения и в виде порошка для приготовления раствора для внутримышечного введения; рабочие названия вакцин – «Гам-КОВИД-Вак» и «Гам-КОВИД-Вак Лио») проводились с 18 июня в военном госпитале им. Бурденко и в Сеченовском университете.
До начала клинических испытаний добровольцев подробно обследовали, в том числе проверили на отсутствие антител к коронавирусу. Затем их на две недели изолировали, чтобы не допустить инфицирования. Добровольцев разделили на две группы – участники первой получили одну дозу вакцины, второй – две. Вакцинация проходила в два этапа – в нулевой день и на 21-й, после вакцинации добровольцы находились в изоляции в стационаре 28 дней, где врачи контролировали их состояние. Также врачи будут контролировать состояние здоровья добровольцев в течение шести месяцев после выписки из стационара.
Директор Института медицинской паразитологии, тропических и трансмиссивных заболеваний Сеченовского университета Александр Лукашев 12 июля сообщил, что безопасность вакцины подтверждена в ходе клинических испытаний. По словам Лукашева, инъекция не вызвала негативной реакции организма, за исключением повышения температуры тела в первые дни после вакцинации.
Вторая фаза испытаний вакцины завершена; третья фаза будет проходить не только в России, но и за рубежом.
11 августа президент РФ Владимир Путин объявил о регистрации в России первой вакцины от коронавируса. Производить препарат планируют на двух площадках: в самом Центре Гамалеи и в компании «Биннофарм». Согласно данным государственного реестра лекарственных средств Минздрава, российская вакцина поступит в гражданский оборот 1 января 2021 года.
В Санкт-Петербургском научно-исследовательском институте вакцин и сывороток ФМБА России создали препарат на основе рекомбинантного белка и наночастиц. Клинические испытания вакцины планируется начать в сентябре-декабре, а в октябре-декабре предоставить регистрационное досье и выйти на промышленное производство в декабре.
Биотехнологическая компания из Санкт-Петербурга Biocad работает над тремя вакцинами от COVID-19. Одну из вакцин на основе везикулярного стоматита Biocad разрабатывает совместно с Государственным научным центром «Вектор». Согласно соглашению, Biocad берет на себя расходы и организационные усилия, связанные с проведением клинических исследований rVSV-вакцины, созданием технологии выпуска препарата и самим производством. Над второй вакциной, на основе аттенуированной (ослабленной) основы вируса гриппа, Biocad работает совместно с Институтом экспериментальной медицины в Санкт-Петербурге. На основе собственных наработок по онковакцинам Biocad разрабатывает инкапсулированную в липосомы мРНК-вакцину против COVID-19.
Федеральный научный центр исследований и разработки иммунобиологических препаратов им. М.П. Чумакова работает над созданием цельновирионной инактивированной (с искусственно ослабленными вирусами) вакцины. Центр успешно завершил доклинические испытания. По словам генерального директора Федерального научного центра исследований и разработки иммунобиологических препаратов им. М.П. Чумакова Айдара Ишмухаметова, в испытаниях принимали участие не только мелкие грызуны, но и приматы, чья реакция на вакцинацию максимально приближена к человеческой. Испытания показали высокую эффективность и безопасность вакцины. Центр имени Чумакова планирует приступить к испытаниям вакцины против COVID-19 в конце августа. В испытаниях примут участие более 100 добровольцев.
Ученые Казанского федерального университета (КФУ) разрабатывают вакцину на основе опубликованного генома вируса с помощью генной инженерии. Профессор кафедры генетики Института фундаментальной медицины и биологии КФУ Альберт Ризванов уточнял, что ученые не могут работать с живым вирусом, поскольку для этого необходима лаборатории высокого уровня биологической безопасности. Ученые могут создать искусственную молекулу ДНК, которая содержит часть вирусного генома. Если такую ДНК-вакцину ввести в организм, то он считает генетическую информацию. Организм начинает синтезировать отдельные вирусные белки, иммунная система распознает их как чужеродные, и вырабатывается защитный ответ. По словам Ризванова, это уникальный подход: ученые КФУ единственные в мире, кто использует комбинацию вирусных генов при создании ДНК-вакцины. 23 июня стало известно, что Казанский федеральный университет приступил к тестированию вакцины против нового коронавируса на лабораторных животных. 24 июля сообщалось, что первый этап апробации вакцины оказался результативным.На втором этапе исследователи анализируют итоги проведения повторной иммунизации. По словам Альберта Ризванова, параллельно с подведением итогов и подтверждением результатов второй иммунизации ученые продолжают работать над второй версией вакцины.
Известно, что на базе биологического факультета МГУ имени М.В. Ломоносова под руководством академика Михаила Кирпичникова разрабатывается прототип поливалентной вакцины против COVID-19, то есть такой, которая бы работала в отношении широкого спектра коронавирусов. Биологи МГУ на основе вирусов растений создали несколько прототипов поливалентной вакцины против коронавирусов, вызывающих такие заболевания как COVID-19, SARS, MERS и коронавирусов летучих мышей, имеющих потенциал преодоления межвидового барьера с человеком.
В Институте биоорганической химии имени Шемякина и Овчинникова под руководством академика Александра Габибова разрабатывается «современная высокотехнологичная вакцина против COVID-19 на основе вирусоподобных частиц с использованием так называемых рекомбинантных фрагментов белков коронавируса». Сообщалось, что в июле-октябре планируется провести доклинические испытания опытных образцов на мышах.
В Институте общей генетики имени Вавилова разрабатывается вакцина, которая несет на своей поверхности три белка коронавируса, что поможет создать также поливалентную вакцину. Работы идут под руководством профессора Козлова, крупнейшего специалиста в области ДНК-вакцин.
В Институте экспериментальной медицины в Санкт-Петербурге разрабатывают «мукозальную вакцину против SARS-CoV-2». Ее разработчики методами генной инженерии встроили в ворсинки на поверхности микробов-пробиотиков S-белок – ключевую молекулу, благодаря которой коронавирус SARS-CoV-2 проникает в клетки. В результате формируется бактерия с иммуногенным белком вируса на поверхности. Вакцину можно будет вводить в организм в виде кисломолочного продукта. В начале июня проводились доклинические испытания этой вакцины.
НИИ гриппа имени А.А. Смородинцева Минздрава России сообщал о наборе добровольцев для испытания вакцины от COVID-19. В сообщении института сказано, что вакцина прошла испытания I и II фазы в Китае. Были привиты 500 добровольцев, доказана ее безопасность и эффективность. Идет набор добровольцев в клиническое исследование вакцины (III фаза). Планируемое начало – середина августа.
В конце июня стало известно, что в Санкт-Петербургском Политехническом Университете Петра Великого (СПбПУ) начали разработку вакцины от коронавируса на основе самореплицирующейся РНК.
Крымский федеральный университет имени В.И. Вернадского начал разрабатывать в начале июля вакцину против нового коронавируса с использованием конструкций на основе тиофосфатных олигонуклеотидов. Ученые пытаются разработать и успешно применить олигонуклеотидную конструкцию в форме «лассо», которая способна одновременно активизировать как клеточный, так и гуморальный иммунитет. Отмечается, что исследователи университета подали заявку на грант Российского фонда фундаментальных исследований на разработку вакцины.
Китай
После того как в Китае произошла вспышка коронавируса, необходимо было как можно скорее приступить к разработке вакцины, местные ученые и профильные компании не стали концентрироваться только на одном виде вакцин, а начали исследовать сразу пять: рекомбинантная субъединичная вакцина, инактивированная вакцина, вакцина на основе аденовирусного вектора, вакцина на основе нуклеиновых кислот и живая аттенуированная гриппозная вакцина.
Первую одобренную для испытаний вакцину разработала исследовательская группа во главе с академиком Военно-медицинской академии КНР Чэнь Вэй. Сообщалось также, что одобрение на клинические испытания инактивированной вакцины получила команда Уханьского института вирусологии при Китайской академии наук и Уханьского института биопрепаратов (входит в состав Sinopharm Group), а также пекинская компания Sinovac Research & Development Co.
15 мая стало известно, что китайские ученые испытали пять различных вакцин от коронавирусной инфекции COVID-19 на более чем 2500 добровольцев. В том числе на первой стадии клинические испытания были проведены на 539 добровольцах, имелись данные о безопасности и выработке антител у испытуемых. На второй стадии испытания вакцины прививки были сделаны 2036 добровольцам. При проведении этих клинических испытаний не получено сообщений о побочных эффектах. Третья фаза клинических испытаний вакцины компании Sinovac пройдет в Бразилии, Индонезии, Бангладеш.
19 июня Государственное управление по надзору за пищевыми продуктами и лекарственными средствами одобрило проведение клинических испытаний рекомбинантной вакцины от COVID-19, разработанной совместно компанией Zhifei Long Kema (дочернее предприятие Chongqing Zhifei Biological Products) и институтом микробиологии Китайской академии наук.
Всемирная организация здравоохранения в апреле заявляла, что ближе всех к завершению находится вакцина, разработанная компанией CanSino Biologics Inc. в Гонконге и Пекинским институтом биотехнологии. 25 июня рекомбинантная вакцина от COVID-19 (на основе аденовирусного вектора) Ad5-nCoV, совместно разработанная CanSino Biologics, Пекинским институтом биотехнологий и Академией военно-медицинских наук Народно-освободительной армии Китая, получила специальное разрешение сроком на один год от управления по вопросам гигиены и здравоохранения объединенных сил материально-технического обеспечения при Центральном военном совете (ЦВС) КНР.
Сообщалось, что первая и вторая фазы клинических тестов указанной вакцины прошли на территории Китая, полученные в результате испытаний данные показали хороший уровень безопасности и высокий уровень гуморального и клеточного иммунного ответа.
В компании подчеркнули, что вакцина Ad5-nCoV в настоящий момент ограничена лишь военным использованием, для более широкого применения необходимо будет отдельное разрешение соответствующего департамента ЦВС КНР.
В конце июня началась первая фаза клинических испытаний китайской РНК-вакцины, которую разрабатывают Академия военно-медицинских наук КНР, Suzhou Abogen Biosciences и Walvax Biotechnology Co. В них участвуют 168 волонтеров, одна возрастная группа – от 18 до 59 лет, другая – от 60 лет. Сообщалось, что пациентам введут по две дозы вакцины в амбулаторном режиме.
США
Администрация США запустила в мае операцию Warp Speed – совместный проект министерства здравоохранения и Пентагона, целью которого является производство 300 миллионов доз вакцины от COVID-19 к январю 2021 года.
Несколько вакцин, разрабатываемых американскими компаниями, считаются перспективными.
В середине марта Национальный институт аллергии и инфекционных заболеваний в Сиэтле (штат Вашингтон) объявил о начале клинических испытаний на людях вакцины от нового коронавируса SARS-CoV-2. Вакцина, получившая название мРНК-1273, разработана Национальным институтом аллергии и инфекционных заболеваний США (NIAID) совместно с биотехнологической компанией Moderna, базирующейся в Кембридже, штат Массачусетс.
Вакцина мРНК-1273 была разработана с использованием генетической платформы, называемой мРНК (мессенджер РНК). Она направляет клетки организма на экспрессию вирусного белка, который, как надеются ученые, вызовет сильный иммунный ответ. Вакцина успешно прошла испытания на животных.
Исследователи надеются, что с ее помощью им удастся настроить иммунную систему человека для борьбы с вирусом.
Для испытания отобрали 45 добровольцев, которым планировалось вводить по две инъекции вакцины с интервалом в 28 дней. Сами дозы у участников эксперимента должны были различаться: 25, 100 и 150 микрограммов. Исследование должно было оценить вакцину на безопасность и способность вызывать иммунный ответ, а также определить оптимальную дозировку.
18 мая компания Moderna объявила о позитивном завершении первой фазы клинических испытаний вакцины от коронавируса. В заявлении Moderna отмечается, что после приема вакцины mRNA-1273 количество антител участников испытаний в зависимости от дозы препарата или превышало соответствующий показатель в крови людей, переболевших COVID-19, или находилось на том же уровне. На начальной стадии препарат показал себя безопасным, он переносится без осложнений.
C 27 июля Moderna приступила к испытаниям вакцины, в которых участвуют около 30 тысяч добровольцев.
Каждый получает дозу потенциальной вакцины в размере 0,1 миллиграмма, через 29 дней инъекция повторяется. Некоторые участники будут привиты препаратом-плацебо.
В июне Moderna опубликовала данные предварительного исследования от COVID-19 на мышах. Сообщалось, что ученые ввели различные количества вакцины шестинедельным мышам, включая дозы, считающиеся недостаточно сильными, чтобы вызвать защитный иммунный ответ.
Затем исследователи подвергли мышей воздействию вируса.
Как подчеркивают ученые, полученные предварительные данные показали, что вакцина является «мощным иммуногенным веществом» и нейтрализующая активность «может быть достигнута с помощью одной дозы». Кроме того, отмечается, что «субпротективные дозы не приводили к усиленной иммунопатологии» после воздействия вируса у мышей, то есть не вызывали более тяжелого течения болезни.
Дальнейшее тестирование показало, что вакцина вызывает мощный ответ нейтрализующих антител. Это то, что необходимо для блокирования вируса, чтобы он не поражал клетки. Вакцина также защищает легкие от заражения коронавирусом без признаков токсического воздействия.
В начале апреля сообщалось, что специалисты Питтсбургского университета в США разработали вакцину от коронавируса и успешно испытали ее на мышах. К тестированию на людях они надеются приступить в ближайшие месяцы. Вакцина получила название PittCoVacc (сокращение от Pittsburgh Coronavirus Vaccine). Вакцина на основе вирусного антигена доставляется в кожу с помощью микроигл, расположенных на поверхности пластыря размером с кончик пальца.
Микроигольный пластырь, внешне похожий на «липучку», содержит 400 крошечных микроигл из сахаров и белков, которые полностью растворяются, не оставляя следов. Результаты исследования на мышах показали, что при такой форме подачи вакцины у животных через две недели вырабатывались антитела, специфичные к SARS-CoV-2, в количествах, которые считаются достаточными для нейтрализации вируса. По словам исследователей, такие пластыри могут быть быстро изготовлены в промышленных масштабах, и их не нужно держать в холоде во время хранения или транспортировки. Это большое преимущество перед традиционной формой вакцины.
В середине мая американская биотехнологическая компания Inovio сообщила о позитивных результатах ее вакцины против COVID-19 в рамках доклинических испытаний, ДНК-вакцина INO-4800 демонстрирует активное реагирование нейтрализующих антител и Т-лимфоцитов на коронавирус SARS-CoV-2.
Вакцина INO-4800 нацелена против главного поверхностного шиповидного белка вируса SARS-CoV-2, из-за которого возникает COVID-19. В рамках исследования было выявлено, что вакцинирование INO-4800 создавало у мышей и морских свинок, на которых проводились испытания, стойкие антитела и Т-лимфоциты, которые реагировали на коронавирус.
В конце июня компания Inovio сообщала об успешном испытании вакцины на обезьянах.
В компании сообщили, что эти результаты доклинических испытаний, а также иммунное реагирование на начальных стадиях клинических испытаний могут позволить уже летом перейти ко второй фазе испытаний.
Фармацевтическая компания Novavax в мае начала первые клинические испытания на людях разработанной ею вакцины от коронавируса. Наночастичковая вакцина, представляющая S-белок SARS-CoV-2 с сапониновым адъювантом получена с использованием запатентованной технологии наночастиц. Вакцина включает в себя адъювант Matrix‑M™ для усиления иммунных реакций и стимуляции высоких уровней нейтрализующих антител. 4 августа Novavax сообщила о двух успешных исследованиях потенциальной вакцины от коронавируса, которую она производит. В одном из исследований 56 волонтеров показали высокий уровень антител на вирус без опасных побочных эффектов. Во втором исследователи обнаружили, что вакцина защищает подопытных приматов от заражения коронавирусом.
Компания Janssen (является структурным подразделением Johnson & Johnson) разрабатывает рекомбинантную вакцину против SARS-CoV-2 – Ad26.COV2-S. В июле было объявлено об успехе доклинических испытаний. В США и Бельгии начались клинические испытания вакцины. Группа добровольцев состоит из 1045 здоровых людей в возрасте от 18 до 55 лет и взрослых в возрасте от 65 лет и старше.
Сингапур
Сингапурская медицинская школа Duke-NUS совместно с расположенной в США Arcturus Therapeutics (компания по производству РНК-препаратов) разрабатывают вакцину LUNAR-COV19, которая основана на самореплицирующейся мРНК. Данные доклинических исследований показали, что уровни нейтрализующих антител в ответ на однократную дозу LUNAR-COV19 продолжают расти в течение 50 дней. 21 июля было объявлено о переходе к клиническим испытаниям.
Таиланд
Тайская группа исследователей под руководством Киата Ракрунгтхама из Центра разработки вакцин Чулалонгкорнского университета в сотрудничестве с университетом Пенсильвании (США) работает над вакциной CU-Cov19. 12 июля ученые завершили тесты на обезьянах и объявили о готовности приступить к тестам на людях-добровольцах в октябре, затем последует вторая фаза испытаний – с декабря по март 2021 года. Третья фаза испытаний на людях требует более 10 тысяч участников, чтобы признать результаты действительными. В связи с относительно небольшим количеством случаев в Таиланде, для проведения третьей фазы испытаний предполагается сотрудничество с Бразилией, Индией и Индонезией. Ученые используют новую технологию, основанную на мРНК.
Индия
В Индии, которая считается одним из крупнейших производителей лекарств в мире, разработкой препарата против COVID-19 занимается несколько компаний. Одна из них – биотерапевтическая компания Bharat Biotech, на счету которой 16 успешно используемых вакцин, в том числе против свиного гриппа (H1N1). Совместно с индийским Советом медицинских исследований и Национальным институтом вирусологии компания разработала вакцину под названием Covaxin.
Вакцина разработана на основе штамма вируса, который был выделен локально и ослаблен в лабораторных условиях.
В начале июля компания Bharat Biotech получила одобрение управления генерального контролера лекарств Индии на клинические испытания разработанного препарата Covaxin на людях.
Вместе с вирусологами из Висконсинского университета в Мадисоне и компанией FluGen, компания Bharat Biotech разрабатывает препарат под названием CoroFlu. По словам представителей компаний-разработчиков, его основу будет составлять экспериментальная вакцина против гриппа от FluGen. В отличие от многих других вакцин, CoroFlu предполагается вводить интраназально, то есть внутрь носа, так как этот способ имитирует естественное попадание инфекции. Кроме того, этот способ введения препарата, как говорят в компании-разработчике, более эффективен и вызывает более сильный иммунный ответ.
В начале июля стало известно, что вторая индийская фирма начала клинические испытания вакцины от коронавируса на людях после получения одобрения от управления генерального контролера лекарств Индии. Препарат разработала компания Zydus Cadila Healthcare Ltd. 5 августа было объявлено о безопасности вакцины. С 6 августа начались испытания этой вакцины на более, чем тысячи добровольцев.
Также в разработку вакцин включились Институт сыворотки Индии (совместно с американской Codagenix), компания Panacea Biotec (совместно с американской Refana), биофармацевтическая компания Indian Immunologicals (совместно с австралийским университетом Гриффита).
Япония
В марте японская фармацевтическая компания «Энджес» (AnGes) объявила о совместной разработке ДНК-вакцины против нового коронавируса COVID-19 с Университетом города Осака. Компания «Энджес» специализируется на разработке ДНК-плазмида HGF, внехромосомного самовоспроизводящегося генетического элемента, и с помощью этой технологии будет создаваться вакцина от коронавируса.
30 июня компания AnGes, Inc приступила к клиническим испытаниям на двух группах из 30 добровольцев. Учредитель компании, ее советник по медицинским вопросам, профессор департамента клинической генотерапии университета Осака Рюити Морисита рассказал, что добровольцы разделены на две группы. Одной группе планировалось вводить меньшее количество вакцины, другой – большее. Вакцинирование планировалось проводить дважды с интервалом в две недели.
Вторая часть исследований с участием 400-500 человек намечена на осень, а к весне AnGes, Inc. рассчитывает выйти на этап промышленного производства вакцины. Главными преимуществами ДНК-вакцины профессор Морисита считает ее безопасность – она не использует патогены, организм создает антитела, реагируя не на патоген, а на ДНК-информацию о нем. Также он отметил возможность произвести вакцину быстро и фактически в неограниченном количестве. Достоинством вакцины ученый считает и то обстоятельство, что ее производство можно гибко подстроить под новые мутации вируса, если таковые произойдут.
Южная Корея / Австралия
12 мая австралийский разработчик вакцин Vaxine Pty заключил соглашение с южнокорейской компанией Medytox о совместной разработке вакцины COVAX-19 от нового коронавируса. 2 июля стало известно, что первые клинические испытания вакцины начались в клиническом исследовательском центре PARC Royal Adelaide Hospital. Сообщалось, что в ходе первой части исследования 40 предварительно отобранным кандидатам в возрасте от 18 до 65 лет будут назначены две дозы вакцины или плацебо с интервалом в три недели. Выработка антител и другие иммунные реакции должны быть проанализированы через две недели после второй инъекции, а данные, как ожидается, будут доступны примерно через два месяца.
Разработкой вакцины от коронавируса также занимается Университет Квинсленда (Австралия) совместно с биотехнологической компанией CSL. Вакцина уже проходит первую фазу клинических испытаний. В них участвуют 120 здоровых добровольцев.
11 июня вакцина от COVID-19, разрабатываемая южнокорейской компанией Genexine Consortium, получила одобрение на проведение клинических испытаний. Разработка представляет собой ДНК-вакцину.
Сообщалось, что исследование будет состоять из первой фазы с участием 40 здоровых добровольцев, за которой последует плацебо-контролируемая фаза IIa оценки двух уровней дозы для обеспечения безопасности и эффективности у 150 пациентов. Ожидалось, что первый этап будет завершен в течение трех месяцев, за которым во второй половине 2020 года последует второй. Данная фаза исследований будет проводиться в нескольких странах.
Канада
Канадская биофармацевтическая компания Medicago, штаб-квартира которой находится в Квебеке, работает над вакциной, основанной на так называемом S-белке, присутствующем на поверхности коронавируса. 14 июля Medicago сообщила, что начинает первую стадию клинических испытаний, которая заключается в случайном наблюдении за 180 здоровыми добровольцами, мужчинами и женщинами в возрасте от 18 до 55 лет. В ходе проверки вакцины будет оценена приемлемая дозировка самой вакцины на растительной основе и в комбинации с вспомогательным стимулирующим веществом.
Вторую стадию клинических испытаний растительной вакцины Medicago планируется начать в октябре. Ожидается, что вакцина будет доступна в 2021 году.
Европа
Биотехнологические компании ReiThera (Италия), Leukocare (Германия) и Univercells (Бельгия) создали консорциум, чтобы ускорить разработку и массовое производство препарата против COVID-19. Вакцина, над которой работают компании, будет создана на основе аденовирусных векторов. Ожидается, что 24 августа 2020 года начнутся испытания вакцины на добровольцах. Испытания будет проводить Национальный институт инфекционных заболеваний Lazzaro Spallanzani в Риме, в них примут участие 90 добровольцев.
Если клинические испытания будут успешны, компании в этом году намерены приступить к производству препарата. Согласно планам консорциума, в начале 2021 года планируется произвести около 6 миллионов доз.
Как заявила представитель компании Leukocare Ева Бауэр, данные, полученные в результате клинических исследований, показывают, что аденовирусные векторы безопасны и «вызывают устойчивой иммунный ответ от одной дозы».
Вакцина против COVID-19, разработанная исследователями из Копенгагенского университета, работающих в рамках европейского консорциума Prevent-Ncov Consortium, была протестирована на мышах. Используемая исследователями технология называется cVLP, что означает «капсидная вирусоподобная частица» (capsid Virus-Like Particle). После введения вакцины мыши производили большое количество антител, способных нейтрализовать вирус SARS-CoV-2. Количество и качество этих антител, индуцированных вакциной, были протестированы непосредственно на вирусе SARS-CoV-2 в двух независимых лабораториях Орхусского университета и медицинском центре Лейденского университета. Исследователи надеются начать клинические испытания до конца года.
Германия
Немецкая фармацевтическая компания CureVac летом начала исследование первой фазы вакцины от COVID-19. Сообщалось, что вакцину планируется ввести 168 добровольцам в Тюбингене, Мюнхене, Ганновере и бельгийском городе Генте. Компания планирует выйти на следующую фазу исследования осенью.
Если тестирование будет успешным, CureVac начнет более масштабные клинические испытания при участии нескольких тысяч человек.
Финансирование данных работ на сумму в более чем 80 миллионов евро намерен поддержать ЕС.
Компания CureVac существует с 2000 года, она была создана на базе университета Тюбингена. Ранее власти ФРГ жестко отреагировали на попытку администрации США выкупить права на новую вакцину против коронавируса, разработкой которой занимается CureVac.
В конце апреля Институт вакцины и биомедицинских препаратов имени Пауля Эрлиха одобрил первое клиническое испытание вакцины против COVID-19, разработанном биоинженеринговой компанией BioNTech из немецкого города Майнц.
Кроме того, BioNTech совместно с фармацевтической компанией Pfizer начала клинические испытания в США – с участием около 8000 человек. Также запланированы клинические испытания вакцины на 30 000 добровольцах. В настоящее время в США и Германии проходит первая и вторая фаза клинических испытаний в общей сложности четырех версий вакцины BNT 162. В июле Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило ускоренную процедуру утверждения двух версий вакцины (BNT162b1 и BNT162b2).
Франция
Национальный институт здравоохранения и медицинских исследований Франции Inserm при поддержке ряда государственных профильных институтов и организаций создает единую платформу вакцин-кандидатов против COVID-19 для проведения их крупномасштабной клинической качественной оценки. Платформа получила название COVIREIVAC.
Транснациональный фармацевтический гигант Sanofi работает над двумя проектами вакцины от коронавируса, один из них – в партнерстве с британским фармацевтическим гигантом GlaxoSmithKline (GSK) и при поддержке связанного с американским Минздравом агентства BARDA, которое уже выделило Sanofi около 30 миллионов долларов. Вакцина основана на технологии рекомбинации ДНК, которая уже применяется при создании антигриппозных вакцин. Начать клинические испытания планируется в сентябре этого года. Одновременно Sanofi ведет разработку и другой вакцины от коронавируса в сотрудничестве с биотехнологической компанией Translate Bio. Данная вакцина создается методом переноса фрагмента РНК, генетического кода вируса. По этой вакцине клинические испытания первой фазы запланированы на период до конца года.
Институт Пастера совместно с группой MSD и компанией Themis Bioscience разрабатывают вакцину на основе аттенуированного штамма кори, который был генетически модифицирован. В конце июня научный руководитель Института Кристоф д`Анфер сообщил, что группа готовится в течение июля начать тестирование на 90 добровольцах во Франции и Бельгии. Организация 2-й и 3-й фаз испытаний планируется совместно с Питтсбургским университетом.
Великобритания
В мае компания AstraZeneca заключила партнерство с Оксфордским университетом для разработки, производства и поставки вакцины от COVID-19. Вакцина ChAdOx1 nCoV-19, разработанная Институтом Дженнера Оксфордского университета совместно с Оксфордской группой по изучению вакцин, использует вирусный вектор на основе ослабленной версии обычной простуды (аденовирус), который содержит генетический материал шиповидного белка SARS-CoV-2. После вакцинации происходит синтез поверхностного шиповидного белка, что приводит к формированию иммунного ответа на COVID-19 при возможном последующем заражении эти вирусом.
В конце мая ученые приступили к третьей фазе клинических испытаний вакцины.
17 июля было объявлено, что в том случае, если разработка AstraZeneca и Оксфордского университета окажется удачной, российская компания «Р-Фарм» возьмет на себя часть производства для поставок на российский рынок и многие другие страны.
Также известно, что вакцину от коронавируса разрабатывают в лондонском университете Imperial College, она может быть готова для применения в первой половине 2021 года. Разработку финансирует правительство Великобритании.
Препарат производится синтетическим путем. По словам одного из разработчиков, профессора Робина Шаттока, после внутримышечной инъекции препарат усиливает РНК и стимулирует иммунный ответ организма на инфекцию. В конце июня начались испытания вакцины на добровольцах. 17 июля началась вторая фаза клинических испытаний.
Биотехнологическая фирма Kentucky BioProcessing, принадлежащая табачной компании British American Tobacco (BAT), работает над созданием вакцины с использованием растений табака. На стадии доклинических испытаний препарат дал положительный иммунный ответ.
Ожидается, что клинические испытания вакцины начнутся 14 сентября 2020 года.
Материал подготовлен на основе информации РИА Новости и открытых источников
Фото: Carl Recine / Reuters
Итальянские ученые изобрели первую в мире вакцину, способную нейтрализовать коронавирус. На их заявление обратил внимание Daily Mail.
Они провели вакцинацию мышам и взяли у них антитела — белки плазмы крови, вырабатывающиеся в качестве ответа на вирус. Выяснилось, что эти антитела способны уничтожать вирус в человеческих клетках в лабораторных условиях. Они успешно предотвращали связывание вируса SARS-CoV-2 с клетками человека и последующее инфицирование.
Разработчики вакцины готовы приступить к тестированию вакцины на людях осенью. «Насколько нам известно, мы первыми в мире продемонстрировали нейтрализацию коронавируса вакциной», — сказано в сообщении ученых. В настоящее время испытанная вакцина считается самой перспективной из всех, созданных в Италии.
По данным на 6 мая, в мире насчитывается более 3,7 миллиона зараженных коронавирусом, из них свыше 259 тысяч человек скончались, более 1,22 миллиона излечились. Наиболее пострадавшие от инфекции страны — США, Испания, Италия, Великобритания и Франция. Россия находится на 7-м месте по числу случаев инфицирования с показателем 165 929 человек.
Что происходит в России и в мире? Объясняем на нашем YouTube-канале. Подпишись!