Физиология и нарушения кислотно-основного состояния (методические материалы к практическим и семинарским занятиям)
Категория:
КазМУНО (АГИУВ). Кафедра анестезиологии и реаниматологии
Информация
Физиология и нарушения кислотно-основного состояния
Методические материалы к практическим и семинарским занятиям
Физиология и нарушения кислотно-основного состояния. Методические материалы к практическим и семинарским занятиям, – 2011. -21 с.
Составители: к.м.н. Батырханова Н.М., ассистент Прмагамбетов Г.К., резидент Иманбекова К.Б., резидент Тлеубаев С.С., под редакцией доцента Чурсина В.В.
Справочное пособие содержит информацию о физиологии кислотно- основного состояния (КОС). Представлена информация о методах лабораторной диагностики нарушений КОС. Перечислены варианты нарушений и методы коррекции. Предназначается для врачей всех специальностей, курсантов ФПК и студентов медвузов.
© Чурсин В.В., Батырханова Н.М., Прмагамбетов Г.К., Иманбекова К.Б., Тлеубаев С.С., 2011 г.
Физиология кислотно-основного состояния
В результате жизнедеятельности клетки в ней постоянно образуются кислоты, которые диссоциируют с освобождением очень активных ионов Н+. Часть этих ионов нейтрализуется буферной системной клетки, другая — буферными системами межклеточной жидкости и крови, а также при функционировании легких, почек, кишечника, печени и др.
Соотношение водородных и гидроксильных ионов во внутренней среде в значительной мере определяет интенсивность окислительно-восстановительных процессов, синтез и расщепление белков, жиров и углеводов, активность ферментов, проницаемость мембран, чувствительность к гормональным стимулам и др. Это соотношение выражается в интегральном показателе рН. Учитывая, что показатель рН часто встречается в медицинской литературе, мы дадим ему более подробную характеристику. Кислотность или щелочность раствора зависит от содержания в нем свободных ионов водорода и концентрации гидроксильных групп.
Если концентрация Н+ > концентрации ОН— — рН кислая
Если концентрация Н+ = концентрации ОН— — рН нейтральная
Если концентрация Н+ < концентрации ОН— — рН щелочная
Эталон нормы – концентрация Н+ = 0,00000001 моль/л в 1 литре химически чистой воды при t0 250С. При этом рН будет нейтральной. Для удобства используют коэффициент рН. Термин «рН» представляет собой аббревиатуру от слов «puissance hydrogen» (puissance по-французски означает сила). Это мера активности или концентрации ионов водорода. рН определяют как отрицательный десятичный логарифм концентрации ионов водорода в моль/л:
pH=-Ig [H+] (конц. Н+) = 7,0
Из этого уравнения следует, что:
рН <7,0 — кислая среда
рН =7,0- нейтральная среда
рН >7,0 – щелочная среда
Для адекватного клеточного метаболизма требуется, чтобы уровень рН крови сохранялся в границах 7,35-7,45, несмотря на постоянную продукцию ионов водорода, которые понижают рН. Даже незначительные нарушения этих границ рН могут иметь неприятные последствия, а снижение рН менее 6,8 и повышение до 7,8 несовместимы с жизнью.
В некоторых случаях лаборатории предпочитают использовать показатель концентрации ионов водорода в нмоль/л, а не рН.
рН 7,4 = концентрация ионов водорода 40 нмоль/л;
рН 7,0 = концентрация ионов водорода 100 нмоль/л;
рН 6,0 = концентрация ионов водорода 1000 нмоль/л.
■ два этих параметра (рН и концентрация Н+) изменяются в противоположных направлениях — если концентрация ионов водорода возрастает, то рН снижается;
■ благодаря логарифмической природе шкалы незначительные изменения рН означают фактически очень существенные изменения концентрации ионов водорода. Например, удвоение концентрации ионов водорода соответствует снижению рН всего на 0,3 единицы.
Факторы, определяющие постоянство рН:
— продукция Н+ за счет катаболизма кислот
— дальнейшее преобразование и распределение кислот в организме
— выведение Н+ из организма
Продукция Н+ происходит в результате расщепления белков, жиров и углеводов. У взрослого человека за сутки вырабатывается 20000 — 22000 ммоль Н+. При перерасчете на НС1 это составит 2 -2,5 л.
В организме продуцируется два вида кислот:
— Н2С03 угольная кислота — летучая кислота, которая выводится через легкие — (слабая кислота, т.к. плохо диссоциирует),
— нелетучие кислоты – H3P04 и Н2SО4 — не выводятся через легкие, но выводятся почками (сильные кислоты, т.к. хорошо диссоциируют).
В норме сильных кислот образуется 50 – 100 ммоль/сутки. При избыточном образовании они вызывают тяжелые нарушения. Это происходит при анаэробном окислении глюкозы.
В норме окисление глюкозы происходит аэробно: С6Н12О2 + 6О2 = 6Н2О + 6СО2 + 38 АТФ
При патологии глюкоза окисляется анаэробно: С6Н12О2 = 2СН2 + 2СН(ОН)СООН + 2 АТФ
В результате образуется избыток кислот и дефицит энергии.
Преобразование и распределение кислот в организме происходит за счет:
-разведения (пассивного механизма);
-действия буферных систем.
Чтобы понять принцип работы химических буферных систем необходимо
разобрать:
Что такое кислоты и основания?
Кислота — это вещество, которое диссоциирует в растворе с высвобождением ионов водорода. Основания (щелочи) присоединяют ионы водорода.
Например, соляная кислота (НС1) диссоциирует на ионы водорода и ионы хлора:
НС1 ↔ Н++Сl—
тогда как бикарбонат (НС03), являющийся основанием, захватывает ион водорода, образуя угольную кислоту:
НСОз + Н+ ↔ Н2С03
Сильные кислоты, такие как соляная, диссоциируют легко, освобождая большое количество водородных ионов, т. е. они имеют очень низкое значение рН. Слабые кислоты диссоциируют хуже, поэтому высвобождается меньше ионов водорода, т. е. они имеют более высокие значения рН, чем сильные кислоты. Иными словами сила кислоты определяется способностью к диссоциации, т.е. степенью, с которой реакция смещается вправо. Водород проявляет кислотные свойства только в ионной форме.
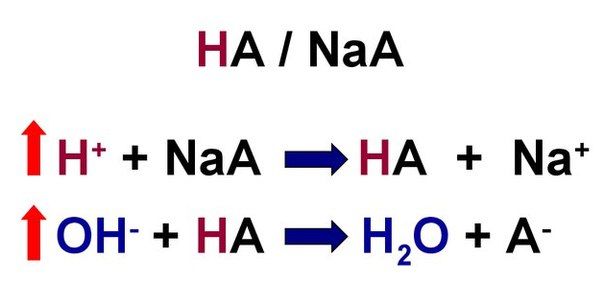
Буферы — это растворы химических композиций, которые способны сглаживать изменения рН, вызываемые добавлением кислоты, при помощи нейтрализации образующихся ионов водорода. Буфер состоит из основания и какой-либо слабой кислоты. Попадание в плазму сильной кислоты вызывает реакцию буферных систем, в результате которой сильная кислота превращается в слабую. То же происходит и при действии на биологические жидкости сильного основания, которое после взаимодействия с буферными системами превращается в слабое основание. В результате указанных процессов изменения рН либо не наступают, либо бывают минимальными.
Бикарбонаты обеспечивают 53% буферной способности крови, небикарбонатные системы — 47%: гемоглобиновый буфер (35%), протеиновый (7%) и фосфатный (5%). Кровь составляет только 1/5 общей буферной ёмкости организма.
1. Бикарбонатная
2. Фосфатная
3. Гемоглобиновая
4. Белковая
Бикарбонатный буфер состоит из угольной кислоты и бикарбоната, в соотношении 1:20
Основная роль данного буфера это перевод сильной кислоты в слабую, сильного основания в слабое:
NаОН + H 2C03 ↔ NаHC03 + Н2О
НСl + NаHC03 ↔ Nа Сl+ H 2C03
↓
С02 + Н2О
Система утрачивает буферные свойства при рН= 6,1, когда соотношение H 2C03 / NаHC03 = 1 /1
Происхождение бикарбонатной буферной системы тесно связано с метаболизмом органического углерода, поскольку конечным продуктом его является СО2 или НСО3— .
Бикарбонатный буфер – главная и единственная система внеклеточной жидкости.
Участие бикарбонатного буфера в выведении H+:
Кислород из вдыхаемого воздуха диффундирует через альвеолы в легкие и соединяется с гемоглобином, который, проявляя буферные свойства, высвобождает ионы водорода:
Освободившиеся ионы водорода буферируются бикарбонатом с образованием угольной кислоты, которая превращается в углекислый газ и воду:
H+ + HC03 ↔ Н2СО3 ↔ С02 + Н2О
Углекислый газ диффундирует из крови в альвеолы и выводится из организма с выдыхаемым воздухом.
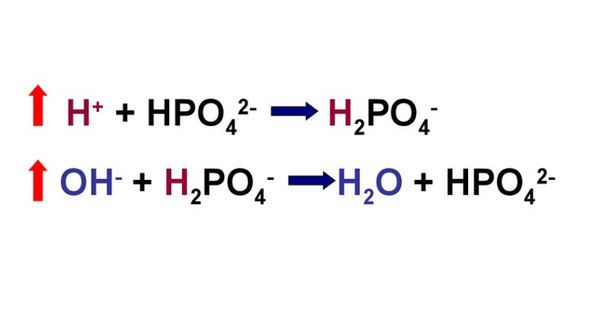
Фосфатная буферная система (1% буферной емкости крови) состоит из фосфорнокислых солей: кислотная часть представлена в виде однозамещенного фосфата натрия NaH2P04, а основная часть представлена двузамещенным фосфатом натрия — Na2HP04. Одноосновные фосфатные соли являются слабыми кислотами, а двухосновные соли имеют ясно выраженную щелочную реакцию.
NaH2P04 / Na2HP04 = 1/4 при рН=7,4
Принцип действия фосфатного буфера аналогичен карбонатному. Непосредственная роль фосфатного буфера в крови небольшая, но ему принадлежит значительная роль в конечной регуляции кислотно-основного гомеостаза и регуляции активной реакции тканей. В крови действие этого буфера сводится к поддержанию и воспроизводству бикарбонатного буфера.
При увеличении в крови кислот и образовании Н2С03 происходит обменная реакция:
H++HC03— + Na2HP04 = NaHC03 + NaH2P04
Избыток Н2С03 ликвидируется, а концентрация НС03 — увеличивается.
Таким образом, удерживается соотношение Н2С03/ NaHCO3= l:20 на постоянном уровне.
02НЬ – слабое основание
С02 – слабая кислота
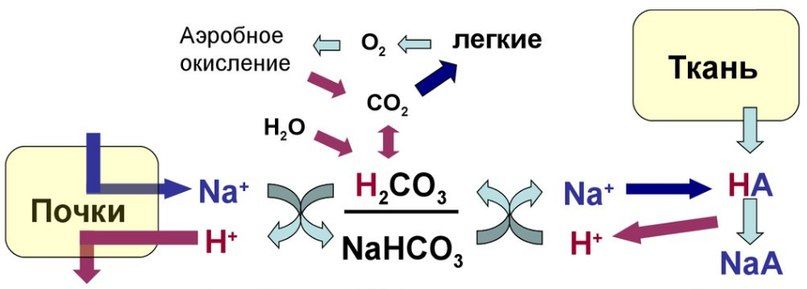
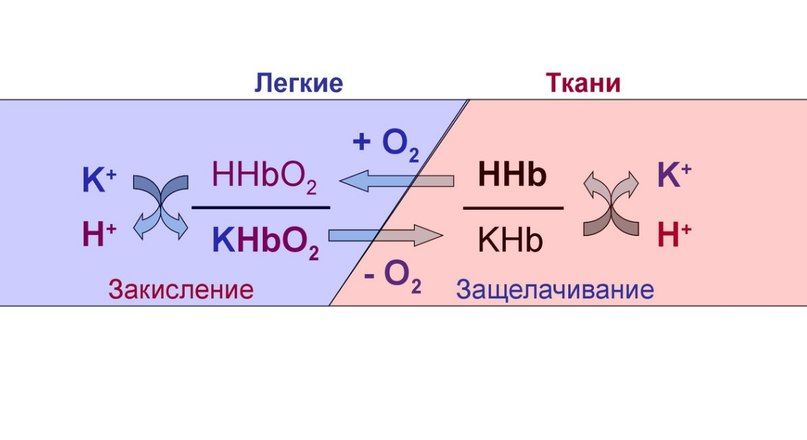
Участие легких в кислотно-основном равновесии состоит в поддержании содержания углекислого газа (С02) в крови. Нормальное количество С02 в крови отражает равновесие между его продукцией в процессе клеточного обмена и выведением легкими с выдыхаемым воздухом. Последовательность событий от продукции С02 в тканях до его элиминации при выдохе выглядит следующим образом (рис. 1):
■ 1. С02 диффундирует из тканей (с высоким содержанием С02) в кровь.
■ 2.В эритроцитах крови С02 превращается в угольную кислоту при участии фермента карбоангидразы. Угольная кислота диссоциирует с образованием бикарбоната и ионов водорода:
С02+ Н20 ↔ Н2С03 ↔ НСО3 — + Н+
■ 3. Так как концентрация бикарбоната растет, часть его диффундирует из эритроцитов в плазму. Ионы водорода (которые, если позволить им накопиться, могут вызвать сильное снижение рН) связываются, с гемоглобином, который освобождается от принесенного кислорода в тканях (гемоглобин в данном случае действует как буфер).
Н+ + 02НЬ ↔ Н+НЬ + 02
■ 4. Когда кровь насыщена кислородом. Кислород из вдыхаемого воздуха диффундирует через альвеолы легких и соединяется с гемоглобином, который, проявляя буферные свойства, высвобождает ионы водорода.
02 + Н+НЬ ↔ Н+ + 02НЬ
■ 5. Освободившиеся ионы водорода буферируются бикарбонатом с образованием угольной кислоты, которая превращается в С02 и воду:
Н+ + НС03— ↔ H2C03 ↔ Н20 + С02
■ 6.С02 диффундирует из крови, где он находится в высокой концентрации, в альвеолы, где концентрация мала, и выводится из организма с выдыхаемым воздухом.
Рис. 1. Доставка 02 к тканям и первые стадии элиминации CO2
Рис. 2. В легких бикарбонат снова превращается в С02 и выводится
Транспорт кислорода из легких к тканям и из тканей к легким обусловлен изменениями, которые воздействуют на сродство кислорода к гемоглобину. На уровне тканей из-за снижения рН это сродство уменьшается (эффект Бора) и вследствие этого улучшается отдача кислорода. В крови легочных капилляров сродство гемоглобина к кислороду увеличивается из-за снижения рС02 и возрастания рН по сравнению с аналогичными показателями венозной крови, что приводит к повышению насыщения артериальной крови кислородом.
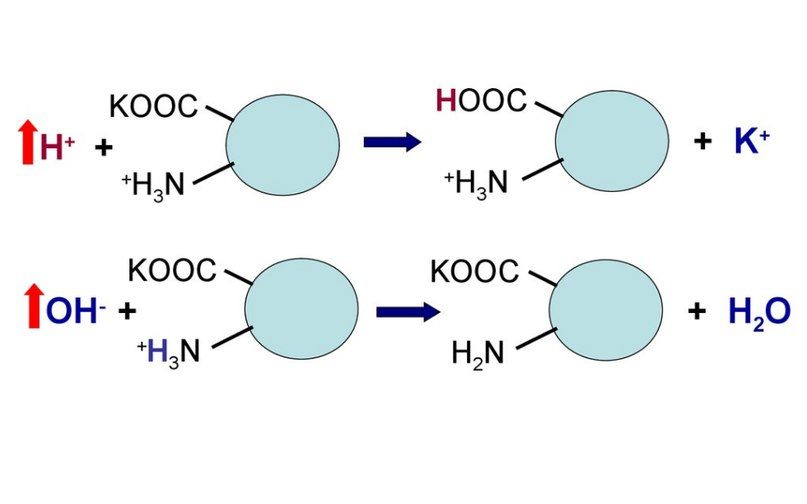
Белки плазмы крови – амфолиты – обладают свойствами кислот. Они составляют большую часть пула анионов плазмы. Изменение содержания альбуминов, протеинов и аномальных белков плазмы оказывает существенное влияние на величину анионной разницы.
Если в крови много Н+, то белки их связывают:
R-CООН + Н+→ R-CООН2
Если в крови много ОН—, то белки отдают Н+ и образуется вода:
R-CООН + ОН—→ R-CОО + Н2О
Выведение Н+ из организма
Почки
Нейтрализация и секреция ионов водорода происходит в результате их обмена с натрием в буферах первичной мочи. Бикарбонатные ионы, которые остаются после выхода Н+ в канальцевую мочу, реабсорбируются в кровь, повышая ее буферную способность. Процесс выведения эпителием почечных канальцев ионов Н+ происходит одновременно с реабсорбцией эквивалентного количества ионов Nа+.
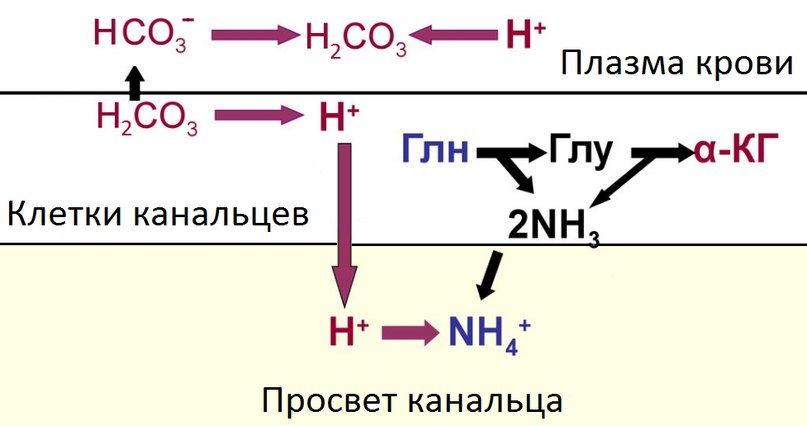
При усиленном выделении почками кислот на уровне дистальных канальцев и собирательных трубок включается механизм аммониогенеза.
Аммиак (NН3) с одной стороны обеспечивает связывание Н+, с другой стороны – выведение анионов сильных кислот в виде аммонийных солей, в составе которых ионы Н+ не оказывают повреждающего действия на эпителий канальцев. Реабсорбция натрия происходит в обмен на выделение как ионов водорода, так и ионов калия. Этот обмен регулируется минералокорикоидами.
При недостатке ионов водорода может усилиться выделение калия, а при избытке – уменьшается.
Желудочно-кишечный тракт.
Клетки слизистой оболочки желудка секретируют Н+ и С1—, а в крови остаются Na+ и НС03—. Защелачивание крови не происходит, так как ионы хлора желудочного сока вновь всасываются в кишечнике. Эпителий слизистой оболочки кишечника секретирует щелочной сок Na+ и НСОз—. При этом в крови остаются Н+ и С1—. Кратковременный сдвиг реакции уравновешивается обратным всасыванием бикарбоната из кишечнике.
В то время, как почки концентрируют и выделяют из организма главным образом Н+ и одновалентные катионы, кишечный тракт концентрирует и выделяет двухвалентные щелочные ионы.
Участие печени
в нейтрализации кислот и оснований возможно за счет нескольких механизмов:
1) Органические кислоты, образующие в процессе метаболизма, в печени превращаются в межуточные и конечные продукты, которые не являются кислотами, или образуют углекислоту, быстро выделяющуюся из легких;
2) Некоторые органические кислоты нейтрализуются, образуя соединение с продуктами белкового обмена (соединение бензойной кислоты с гликогеном);
3) Молочная кислота нейтрализируется в печени, превращаясь в гликоген. Этот процесс имеет значение после усиления мышечной работы, когда в кровь поступает значительное количество молочной кислоты;
4) Неорганические кислоты задерживаются в печени, нейтрализуются и удаляются вместе с желчью. Также удаляются вместе с желчью и основания;
5) В печени происходит нейтрализация кислот аммиаком, образующимся при дезаминировании аминокислот и некоторых других продуктов белкового обмена.
Первичные изменения КЩС и компенсаторные реакции
Компенсаторные реакции немедленного типа
Дыхательная компенсация срабатывает при метаболических нарушениях (ацидоз, алкалоз).
Через легкие выводится в большей или меньшей степени С02. Это зависит от возбуждения или угнетения дыхательного центра.
Возбуждает дыхательный центр увеличение рС02 и снижение рО2 , уменьшение концентрации гидрокарбоната.
Угнетает дыхательный центр снижение рС02 и увеличение рО2 , увеличение концентрации гидрокарбоната.
Снижение уровня НСО3– в плазме крови (метаболический ацидоз), возникающее первично, компенсируется увеличением легочной вентиляции и снижением рС02, при этом соотношение рС02 /НСО3– остается неизменным.
При тяжелом метаболическом ацидозе стимуляция вентиляции легких доходит до крайнего предела (рС02 ниже 20 мм рт.ст. и даже ниже 10 мм рт.ст.), и дальнейшая компенсация становится невозможной.
Увеличение содержания НСО3– в плазме крови (метаболический алкалоз), возникающее первично, компенсируется снижением легочной вентиляции и увеличением рС02. Как правило, выраженный дыхательный ацидоз не развивается. Тем не менее, при выраженном метаболическом алкалозе существует опасность гиповентиляции и гиперкапнии.
Компенсаторные реакции начинаются сразу же при изменении содержания НСО3–. Максимум компенсации достигается через 12- 24 часа.
Компенсаторные реакции замедленного типа
Основной компенсаторный механизм при дыхательных нарушениях. Суть данного механизма сводится к выведению в большей или меньшей степени Н+ нелетучих кислот и также реабсорбции NаHC03 — обеспечивается функцией почек (аммониогенез, титрование Н+, реабсорбция).
Первичное снижение рС02 (дыхательный алкалоз) способствует подавлению реабсорбции бикарбоната в канальцах почек и задержке ионов Н+, в результате чего снижается содержание НСО3– в плазме крови и компенсаторно развивается метаболический ацидоз.
Первичная гиперкапния (дыхательный ацидоз) сопровождается увеличением реабсорбции бикарбоната и усилением выведения ионов Н+, компенсаторно развивается метаболический алкалоз.
Эти компенсаторные реакции в отличие от реакций немедленного типа происходят длительное время – 6 -12 часов и достигают максимума через несколько суток. Быстрое возрастание рС02 – острый дыхательный ацидоз не компенсируется почками и может привести к летальному исходу без заметного содержания бикарбоната в крови. В отличие от острого, медленно прогрессирующий дыхательный ацидоз (хронический) компенсируется увеличением уровня бикарбоната в крови и прямой угрозы для жизни не представляет.
Определение первичного нарушения КЩС
Снижение или повышение одного показателя — рН крови – свидетельствует об ацидозе или алкалозе, но не дает исчерпывающего ответа на вопрос, какой компонент КЩС нарушен: респираторный или метаболический.
Если же интерпретируются два показателя (рН и рС02), то определение первичности нарушения КЩС становится возможным (таб. 1).
Таблица 1. Определение первичности нарушения КЩС
|
рН артериальной крови (норма 7,35 – 7,45) |
рС02 (норма 35 -45 мм рт.ст.) | Первичное нарушение |
| Снижен | Повышено | Дыхательный ацидоз |
| Снижен | Норма или снижено | Метаболический ацидоз |
| Повышен | Повышено или норма | Метаболический алкалоз |
| Повышено | Снижено | Дыхательный алкалоз |
| Норма | Понижено |
Смешанная форма дыхательного алкалоза и метаболического ацидоза |
| Норма | Повышено |
Смешанная форма дыхательного ацидоза и метаболического алкалоза |
Кислотно-основной гомеостаз крови характеризуют следующие показатели:
рН — показатель активной реакции крови; суммарно отражает функциональное состояние дыхательных и метаболических компонентов и изменяется в случае превышения возможностей всех буферных систем (в норме 7,35 — 7,45).
рСО2 (мм рт. ст.) — напряжение углекислоты в крови; единственный дыхательный показатель КОГ, отражающий функциональное состояние системы дыхания, изменяющееся при ее патологии и в результате компенсаторных реакций при метаболических сдвигах (в норме 35-45 мм рт.ст. в артериальной крови).
АВ (ммоль/л) — истинные бикарбонаты крови (aktual bikarbonate); концентрация ионов угольной кислоты, НС03— при физическом состоянии крови в кровеносном русле, т. е. определенное без соприкосновения с воздухом при температуре 38°С (в норме 21,8-27,2 ммоль/л).
SВ (ммоль/л) — стандартный бикарбонат (standart bikar-bonate); концентрация бикарбонатных ионов (НС03—, измеренная при стандартных условиях: рС02 — 5,3 кПа (40 мм рт. ст.), при температуре 38°С и полном насыщении гемоглобина кислородом. Характеризует смещение ионов бикарбонатной системы.
Этот показатель считается более ценным в диагностическом отношении, чем истинный бикарбонат, поскольку отражает только метаболические сдвиги (в норме 21,6—26,9 ммоль/л).
ВВ (ммоль/л) — буферные основания крови (buffer base); общая концентрация буферных ионов бикарбонаты, белки, гемоглобин в полностью оксигенированной крови. Диагностическое значение этого показателя небольшое, т.к. он меняется в зависимости от рС02, концентрация гемоглобина (в норме 43,7-53,5 ммоль/л).
BE (ммоль/л) — избыток или недостаток буферных оснований (base excess). Характеризует сдвиг ионов всех буферных систем и указывает на природу нарушений кислотно-основного гомеостаза. Отрицательное значение BE отражает дефицит оснований или избыток кислот. При метаболических сдвигах КОГ крови смещение BE будет выражено более значительно, чем при дыхательных нарушениях (в норме BE = -3 — + 3 ммоль/л).
АР- анионная разница. В основе клинического применения показателя АР лежит предположение, что любой раствор, включая плазму, должен быть электронейтральным, т.е. сумма катионов равна сумме анионов. Плазма содержит один главный измеряемый катион Na+ и два главных измеряемых аниона СI— и НСОз—. Вклад других неизмеряемых анионов (НА) и катионов (НК) невелик (таб. 2). Из этого следует, что сумма измеряемых и неизмеряемых анионов равна сумме измеряемых и неизмеряемых катионов:
НА + (СI— + НСОз—) = НК + Na+
Таблица 2. Анионная разница
Пользуясь данными таблицы можно рассчитать АР:
АР = НА – НК = 23 – 11 = 12 мэкв/л
АР = НА – НК = Na+- (СI— + НСОз—)
В случаях увеличения Н+ неравенство между измеряемыми в плазме концентрациями катионов и анионов выйдет за пределы нормального диапазона 9 – 13 мэкв/л.
Показатель АР может быть полезен для выявления этиологии метаболического ацидоза.
Как правило, чем больше АР, тем легче определить причину ацидоза.
Высокая АР характерна для лактат-ацидоза, вызванного анаэробным гликолизом. Диабетический кетоацидоз и уремия также сопровождается увеличением АР. Если при высокой АР уровень лактата, кетона и креатинина нормальный, наиболее вероятно, что причиной ацидоза является прием токсичных веществ (метанол, паральдегид, этанол, этиленгликоль, лекарственные средства). Высокий уровень салицилатов в плазме сопровождается значительным увеличением АР.
Классификация нарушений КЩС
1. Простые нарушения:
Ацидоз:
— метаболический
— респираторный
Алкалоз:
— метаболический
— респираторный
2.1 Однонаправленные: метаболический и дыхательный ацидоз и алкалоз
2.2 Разнонаправленные:
— метаболический ацидоз и дыхательный алкалоз
— метаболический алкалоз и дыхательный ацидоз
Значения рН остаются в пределах нормы (рН=7,35 — 7,45), содержание бикарбонатов и СО2 изменяется в зависимости от направленности метаболических и респираторных сдвигов.
Кроме изменений в содержании бикарбонатов и СО2 изменяется и рН, но в незначительных пределах + 0,04 (рН=7,31 – 7,49)
рН < 7,30 – некомпенсированный ацидоз;
рН > 7,50 – некомпенсированный алкалоз.
Метаболический ацидоз
Метаболический ацидоз возникает вследствие существенного снижения уровня бикарбоната в организме.
1. Увеличение продукции нелетучих кислот.
Усиленная продукция кислых метаболитов (так называемых кетокислот — (3-гидроксибутирата и ацетоацетата) является одной из характерных особенностей неконтролируемого или плохо контролируемого инсулинзависимого диабета. При этом состоянии, называемом диабетическим кетоацидозом, количество бикарбоната в крови значительно снижается из-за его использования для нейтрализации избытка кислот.
В клетках, которые в значительной мере лишены кислорода и, поэтому, не могут метаболизировать (окислять) глюкозу происходит накопление лактата. Такое существенное накопление лактата в крови в количествах, достаточных для развития метаболического ацидоза, происходит, если ткани неадекватно перфузируются кровью, а следовательно и недостаточно оксигенируются.
Наиболее яркой причиной лактоацидоза при нарушении перфузии тканей является гиповолемический шок. Кроме того, лактоацидоз может возникать при почечной или печеночной недостаточности, диабете, сепсисе и лейкемии.
2. Увеличение потерь оснований.
Бикарбонат секретируется в полость тонкого кишечника для осуществления пищеварения и абсорбируется в нижних отделах желудочно-кишечного тракта. Если реабсорбции не происходит, он теряется с фекалиями.
Любые заболевания пищеварительного тракта (например, тяжелая диарея) могут привести к потерям бикарбоната из организма в количествах, достаточных для развития метаболического ацидоза.
Также потеря бикарбонатов может быть связана с почечной недостаточностью (проксимальный канальцевый ацидоз – почечный ацидоз II типа). Ухудшение реабсорбции Nа+ приводит появлению щелочной реакции мочи. Кроме этого, проксимальный канальцевый ацидоз характеризуется снижением уратов, фосфатов и калия в сыворотке крови, глюкозурией и аминоацидурией.
С помощью величины АР можно отличить потери НСОз— при диарее от потерь НСОз—, вызванных почечным канальцевым ацидозом таб. 3.
Таблица 3. Анионная разница по (П.Марино, 1998)
|
АР мочи АР = (Nа+ + К+) – СI- |
рН мочи | диагноз |
|
Отрицательная Положительная Отрицательная |
<5,5
>5,5 >5,5 |
Патологии нет Почечный канальц. ацидоз Диарея |
3. Увеличение поступлений в организм кислот извне.
Злоупотребление кислой пищей, прием внутрь соляной кислоты, введение в больших количествах старой консервированной крови
4. Уменьшение выведения ионов Н+ через почки.
В нормальных условиях почки выводят Н+ в виде титруемой кислоты (фосфаты, сульфаты) и аммиака. Этот механизм может быть нарушен при заболеваниях почек, недостаточности надпочечников, дистальном почечном канальцевом ацидозе и гиперальдостеронизме. При почечной недостаточности, уменьшении числа функционирующих нефронов адекватная фильтрация и выведение Н+ отсутствуют.
При почечном ацидозе I типа (дистальный канальцевый ацидоз) секреция Н+ в дистальных канальцах нарушается. Поскольку экскреция Н+ в дистальных канальцах зависит от обмена Nа+ , уменьшение объема жидкости способствует нарастанию ацидоза. Посредством такого же механизма, связанного с уменьшением поставки Nа+ в канальцы почек, адреналиновая недостаточность и селективный гипоальдостеронизм также приводят к ухудшению экскреции Н+. При этом метаболический ацидоз сочетается с другими формами нарушений электролитного обмена: гиперкалиемией, гипонатриемией, гиперкальциемией.
Снижение уровня НСО3– в плазме крови (метаболический ацидоз), возникающее первично, компенсируется увеличением легочной вентиляции и снижением рС02, при этом соотношение рС02 /НСО3– остается неизменным.
Увеличение содержания кислот буферируется бикарбонатным буфером:
НС1 + H 2C03/NаHC03 ↔ Nа Сl+ H 2C03
↓
С02 + Н2О
Диагностические критерии:
1. При сниженном рН нормальный или пониженный уровень рСО2 указывает на первичный метаболический ацидоз;
2. При нормальной величине рН пониженный уровень рСО2 указывает на смешанную форму дыхательного алкалоза и метаболического ацидоза;
3. При нормальной величине рН нормальный уровень рСО2 может свидетельствовать о том, что показатели КЩС находятся в пределах нормы, но не исключается возможность смешанных метаболических алкалозов/ацидозов.
В этих случаях определяют АР и по этому показателю судят об изменениях КЩС.
4. Дефицит оснований – АВ, ВЕ, ВВ, SВ.
Клинические формы ацидоза
Лактат – ацидоз
Этиопатогенез.
1. Снижение оксигенации тканей – тканевая гипоксия. Наибольшее значение придают циркуляторным нарушениям (кардиогенный, септический, гиповолемический шок). Наличие всех форм гипоксии теоретически способствует развитию лактат-ацидоза. Остановка сердца сопровождается анаэробным обменом веществ и лактат-ацидозом;
2. Нарушения функции печени снижают ее способность к превращению молочной кислоты в глюкозу и гликоген.
3. Недостаток тиамина (витамин В1) у больных, злоупотребляющих алкоголем ведет к угнетению окисления пирувата в митохондриях и способствует накоплению молочной кислоты.
4. Повышение правовращающего изомера молочной кислоты (D-лактат-ацидоз), неопределяемого стандартными лабораторными методиками. Это изомер образуется в результате действия микроорганизмов, расщепляющих глюкозу в кишечнике. Чаще всего встречается у больных после обширных операций на кишечнике, при дисбактериозе, нарушениях функции ЖКТ. По-видимому, это наиболее распространенное нарушение КЩС, но оно часто не диагностируется (П.Марино, 1998);
5. Не исключается возможность лактат-ацидоза при длительных инфузиях адреналина и других сосудосуживающих средств.
6. Лактат-ацидоз может развиться в случаях использования натрия нитропруссида, при метаболизме которого образуются цианиды, способные нарушать процессы окислительного фосфорилирования.
Диагностика лактат-ацидоза:
— наличие метаболического ацидоза, связанного с повышенной АР;
— выраженный дефицит оснований;
— АР>30 мэкв/л, в то время как другие причины, вызывающие ацидоз (кетоацидоз, почечная недостаточность, введение токсических веществ), отсутствуют;
— уровень молочной кислоты в венозной крови превышает 2 мэкв/л. Этот показатель отражает интенсивность образования лактата в тканях.
Устранение причины лактат-ацидоза.
Введение натрия бикарбоната показано при рН<7,2, содержании НСОз— <15 ммоль/л. Расчет примерной дозы натрия бикарбоната можно провести по следующей формуле:
Дефицит НСОз—(ммоль) = 0,3 * масса тела (кг) * ВЕ = мл 8,5%р-р соды
Для 3% соды: ВЕ*0,8*масса тела
Для 4% соды: ВЕ*0,6*масса тела
Для 5% соды: ВЕ*0,5*масса тела
Вначале устраняют половину выявленного дефицита НСОз путем внутривенного введения раствора в течение 30 минут. Затем под контролем содержания НСОз в сыворотке крови продолжают коррекцию в течение 4 – 6 часов.
Пример:
В данном случае рН ниже нормы — обозначается как некомпенсированный ацидоз. Далее оцениваем газовый состав крови: уровень рО2 для артериальной крови несколько повышен, но рСО2 снижен. Учитывая дефицит оснований и повышенный лактат можно сделать вывод, что это метаболический лактат-ацидоз, при котором включена немедленная компенсация в виде гипервентиляции.
Кетоацидоз.
В условиях выраженного дефицита инсулина блокируется поступление глюкозы в мышцы и жировую ткань, снижается уровень глюкозы в клетках, ткани испытывают «энергетический голод». Это ведет к гиперсекреции контринсулярных гормонов – соматотропина, глюкагона, кортизола, адреналина. Под влиянием этих гормонов стимулируется гликогенолиз, глюконеогенез и липолиз. В результате липолиза жиры расщепляются до свободных жирных кислот, которые становятся источником энергии и кетоновых тел. В условиях дефицита инсулина происходит чрезмерное образование кетоновых тел, развивается кетоацидоз.
— слабость, жажда, тошнота;
— диабетическая прекома;
— диабетическая кома.
— гипергликемия
— глюкозурия
— метаболический ацидоз (снижение рН, НСОз, рСО2, выраженный дефицит оснований)
— ацетон в плазме
— ацетонурия
— гиперосмолярность плазмы > 300 мосм/л
Первоначальная доза инсулина 10 ЕД в/в. Последующую инфузию инсулина в изотоническом растворе натрия хлорида или 5% раствре глюкозы проводят со скоростью 0,1 ЕД/кг/час.
Дефицит внеклеточной и внутриклеточной жидкости при кетоацидозе может достигать 10% массы тела. Лечение следует начинать с введения изотонических растворов, содержащих Na+ и CI—. Опасность чрезмерного введения кристаллоидов заключается не только в перегрузке объёмом, но и в дисбалансе концентраций натрия и глюкозы. Поэтому необходим динамический контроль этих веществ и при необходимости своевременная коррекция.
Потери К+ при кетоацидозе достигают 200 – 700 ммоль и продолжаются по мере устранения ацидоза. Проводя коррекцию гипокалиемии необходимо учитывать не только дефицит, но и потребность. Представлена формула расчета дефицита К+:
Дефицит калия (ммоль) = масса больного (кг) х 0,2 х (4,5 – К+ плазмы)
Рекомендуется введение натрия бикарбоната при снижении рН < 7,2 и снижении АДсист ниже 90 мм рт.ст., для предупреждения дальнейших электролитных нарушений и гемолиза. Но введение раствора соды должно быть более осторожным, чем при лактат-ацидозе, рекомендуется вводить 1/2 расчетной дозы.
— превращение этанола в процессе метаболизма в печени в ацетальдегид с образованием НАД-Н, способствующего выработке кетоновых тел;
— сопутствующее голодание, сопровождающееся усилением кетогенеза и кетонемией;
— обезвоживание, ведущее к олигурии и снижению экскреции кетоновых тел с мочой.
Алкогольный кетоацидоз обычно развивается через 1 – 3 дня после чрезмерного потребления спиртных напитков. Как правило, уровень глюкозы и кетоновых тел повышается не очень высоко.
Показано в/в введение изотонического раствора натрия хлорида и 5% глюкозы.
Глюкоза угнетает образование кетоновых тел в печени, а солевые растворы повышают выведение их с мочой. Коррекцию калия проводят по содержанию его в сыворотке крови. натрия бикарбонат применим только если рН < 7,2 и снижении АДсист ниже 90 мм рт.ст..
Пример:
Интерпретация анализа начинается с рН. В данном случае рН ниже нормы и обозначается как некомпенсированный ацидоз. Далее оцениваем газовый состав крови: уровень рО2 для венозной крови нормальный, однако сделать заключение о наличие гипоксемии нельзя, для этого необходимо определить рО2 в артериальной крови. Но с учетом нормального уровня лактата, можно сделать вывод, что дефицита О2 нет, идет аэробный гликолиз. Генез ацидоза метаболический и данное заключение можно сделать по уровню дефицита оснований.
Снижение уровня бикарбоната может быть связано с метаболическим ацидозом или развившейся почечной недостаточностью, это можно сказать с учетом анамнестических и клинических данных.
— Потеря нелетучих кислот
Тяжелая и длительная рвота желудочным соком (он кислый) приводит к потере НСI из организма. Это причины метаболического алкалоза, ассоциированного со стенозом привратника — состояния, при котором затрудняется продвижение желудочного содержимого в тонкий кишечник.
— Потеря ионов Н+
Гипокалиемия увеличивает проксимальную канальцевую реабсорбцию НСОз и повышает дистальную канальцевую секрецию Н+. Повышение уровня албдостерона увеличивает секрецию Н+.
— Избыточное введение бикарбоната натрия.
В данном случае алкалоз развивается при неконтролируемом введении бикарбоната, цитрата, лактата или ацетата.
Компенсаторные механизмы:
Увеличение содержания НСО3– в плазме крови (метаболический алкалоз), возникающее первично, компенсируется снижением легочной вентиляции и увеличением рС02. Как правило, выраженный дыхательный ацидоз не развивается. Тем не менее, при выраженном метаболическом алкалозе существует опасность гиповентиляции и гиперкапнии.
NаОН + H 2C03/NаHC03 ↔ 2NаHC03 + Н2О
— НСОз в артериальной крови более 25 ммоль/л, в венозной крови – более 30 ммоль/л;
— рН выше нормального уровня;
— рСО2 нормальное или повышенное, в наиболее тяжелых случаях может быть сниженным;
— при гипохлоремическом алкалозе – СI менее 100 ммоль/л;
— часто бывает гипокалиемия.
1.Устранение основной причины алкалоза;
2.Восполнение дефицита: Дефицит СI (моль/л) = 0,27* масса тела (кг) * (100 – фактическое содержание СI)
Необходимый объём изотонического раствора натрия хлорида может быть определен по формуле: NаСI (л) = дефицит СI / 154, где 154 – содержание СI (моль/л) в 1 л 0,9% раствора натрия хлорида;
3.При потерях НСI необходимо в/в раствора НСI. Обязательное условие для его назначения – нормальное содержание жидкости в организме и нормальная концентрация К+ в сыворотке крови. Дефицит водорода определяют по следующей формуле:
Дефицит Н+ = 0,5 * масса тела (кг) *
(фактическое содержание HC03 – желаемое содержание HC03)
В 1 л 0,1 нормального раствора HC03 содержится 100 ммоль Н+. скорость введения раствора НСI – 0,2 ммоль/кг/час.
Максимальная суточная доза раствора НСI = 100 ммоль.
При неосложненном метаболическом алкалозе содержание HC03 в сыворотке крови менее 35 ммоль/л считают относительно безопасным.
4.Устранение гипокалиемии (см. выше).
Пример:
В данном случае рН выше нормы и обозначается как некомпенсированный алкалоз. Далее оцениваем газовый состав крови: уровень рСО2 несколько повышен, а рО2 в пределах нормы, следовательно алкалоз не респираторного происхождения. Генез алкалоза однозначно метаболический, что подтверждает избыток оснований.
Дыхательный ацидоз.
— Острая дыхательная недостаточность;
— Хроническая дыхательная недостаточность.
Острый дыхательный ацидоз.
Острый дыхательный ацидоз представляет угрозу для жизни больного, характеризуется первичным острым накоплением СО2 в жидких средах организма из-за снижения альвеолярной вентиляции, ограничивающей элиминацию СО2. Однако наряду с увеличением содержания в крови СО2, как правило наблюдается снижение рО2 в артериальной крови.
Первичная гиперкапния (дыхательный ацидоз) сопровождается увеличением реабсорбции бикарбоната и усилением выведения ионов Н+ почками, компенсаторно развивается метаболический алкалоз. Но эта компенсаторная реакция относится к реакции замедленного типа, которая происходит длительное время (6-12 часов) Клетки почечных канальцев богаты ферментом карбоангидразой, которая катализирует синтез угольной кислоты из углекислого газа и воды. Угольная кислота диссоциирует с освобождением бикарбоната, который выходит в кровь (для восполнения бикарбонатного буфера), и ионов водорода, которые эксретируются с мочой.
В крови действие фосфатного буфера сводится к поддержанию и воспроизводству бикарбонатного буфера. При увеличении в крови кислот и образовании Н2С03 происходит обменная реакция:
H++HC03— + Na2HP04 = NaHC03 + NaH2P04
Избыток Н2С03 ликвидируется, а концентрация НС03— увеличивается.
Остро возникшее увеличение содержания СО2 в крови в первую очередь проявляется изменениями функции ЦНС и в меньшей степени сердечно-сосудистой системы. Потеря сознания является результатом интраневрельного ацидоза, усиления мозгового кровотока и увеличения ВЧД, за счет гиперкапнии и дилатации сосудов мозга. Системное сосудорасширяющее действие гиперкапнии проявляется гиперемией кожных покровов, повышенной потливостью, тахикардией.
Восстановление адекватной вентиляции легких и оксигенации крови, под контролем рСО2 и рО2 в артериальной крови. Одновременно проводят лечение основного заболевания, вызвавшего острый дыхательный ацидоз.
Хронический дыхательный ацидоз.
Хронические обструктивные заболевания легких.
Хронический дыхательный ацидоз развивается длительное время, компенсация может быть полной, и тогда рН не выходит за пределы нормы при повышенном рСО2 в артериальной крови и соответствующем возрастании НСО3. При отсутствии достаточных механизмов компенсации хронический дыхательный ацидоз может быть субкомпенсированным. Обычно повышение рСО2 сопровождается умеренным снижением рН и увеличением уровня НСО3. Из организма при этом выводятся Н+,CI— и NН4CI, обладающий свойствами сильной кислоты. Компенсаторный характер метаболического алкалоза очевиден. Несмотря на почечную компенсацию, дыхательные нарушения могут прогрессировать.
Хронический дыхательный ацидоз может перейти в острый, и тогда он представляет угрозу для жизни больного.
Профилактика и лечение основного заболевания.
Пример:
В данном случае рН ниже нормы — обозначается как некомпенсированный ацидоз. Оцениваем газовый состав крови: уровень рО2 для венозной крови нормальный, однако сделать заключение о наличие гипоксемии нельзя, для этого необходимо определить рО2 в артериальной крови. Но с учетом нормального уровня лактата, можно сделать вывод, что дефицита О2 нет, идет аэробный гликолиз. Но повышенный уровень рСО2 говорит о дыхательном ацидозе. Тактика коррекции будет зависеть от клиники.
Дыхательный алкалоз.
— нарушения функции ЦНС;
— болевой синдром;
— возбуждение;
— ИВЛ в режиме гиповентиляции.
Первичное снижение рС02 (дыхательный алкалоз) способствует подавлению реабсорбции бикарбоната в канальцах почек и задержке ионов Н+, в результате чего снижается содержание НСО3– в плазме крови и компенсаторно развивается метаболический ацидоз.
Патофизиологические изменения.
Доказано, что острая гипокапния сопровождается снижением содержания бикарбонатов и концентрации Н+ не только в артериальной крови, но и в цереброспинальной жидкости. Острая гипокапния снижает мозговой кровоток, что приводит к гипоксии мозга и увеличению образования в мозге лактата.
При острой гипокапнии возможны значительное снижение сердечного выброса, повышение ОПСС, что ведет к значительному уменьшению перфузии тканей и увеличению содержания лактата в плазме.
Обычными признаками острого алкалоза являются тахипноэ и одышка. При хроническом алкалозе частота дыхания может оставаться нормальной при повышенном дыхательном объёме. Признаки дыхательного алкалоза не специфичны и проявляются нарушением нейромышечной функции (парестезии, судороги, тремор).
Специального лечения не требуется, важно выявить и устранить основную причину, вызвавшую это нарушение.
Пример:
В данном случае рН выше нормы и обозначается как некомпенсированный алкалоз.
Учитывая, что рСО2 ниже нормы, уровень лактата в норме и нет избытка оснований, можно говорить о чистом дыхательном алкалозе. Тактика коррекции будет зависеть от клиники.
При гипокапнии и одновременном повышении уровня лактата с метаболическим ацидозом, необходимо думать о циркуляторной или тканевой гипоксии – низкой продукции углекислоты тканями при анаэробном гликолизе.
Это чрезвычайно опасная ситуация, сопровождающаяся нормальной сатурацией и нормальным напряжением кислорода, что успокаивает врача. Подтверждением этому опасному состоянию служит низкая артерио-венозная разница по кислороду.
Литература
1. Бунятян А.А., Рябов Г.А., Маневич А.3. Анестезиология и реаниматология. 2-е изд. перераб. и доп. М., Медицина 1984
2. Дэвид М.Габа, Кевин Дж.Фиш, Стивен К.Хауард. Критические ситуации в анестезиологии. Перевод с англ. –М.М. -2000 г.
3. Малышев В.Д. Интенсивная терапия острых водно-электролитных нарушений. М.:Медицина,1985. 192 с.
4. Малышев В.Д. Интенсивная терапия. Реанимация. Первая помощь: Учебное пособие. — М.: Медицина.— 2000.— 464 с
5. Уилкинсон А.У. Водно-электоролитный обмен в хирургии / Пер. с англ. М.: Медицина 1974
6. Шмидт Р., Тевс Г. /ред./ Физиология человека. /пер. с англ./ М., 1986, т.3.
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Ацидоз и алкалоз – это термины, используемые для описания ненормальной ситуации, вызванной избытком кислот или щелочей (оснований) в крови. Этот дисбаланс вызван рядом состояний или заболеваний.
Что такое ацидоз и алкалоз
Чтобы обеспечить нормальное функционирование метаболических процессов и снабжение тканей достаточным количеством кислорода, нормальный pH крови должен поддерживаться в узком диапазоне 7,36-7,44.
- Ацидоз — это состояние с избытком кислот в крови, что приводит к падению pH крови ниже 7,36.
- Алкалозом называют избыток оснований в крови с последующим повышением pH крови выше 7,44.
Повлиять на регулирование pH крови и привести к тому, что pH крови окажется за пределами диапазона здоровых людей могут многие состояния и заболевания. Равновесие можно восстановить, увеличив выведение и / или уменьшив потребление этих веществ.
Причины развития ацидоза и алкалоза
Во время метаболизма образуется большое количество кислот, которые необходимо нейтрализовать и / или удалить, чтобы поддерживать нормальный pH. Например, угольная кислота, образующаяся из двуокиси углерода (CO 2) и воды. Углекислый газ образуется в организме в процессе метаболизма глюкозы и жиров. Также образуются меньшие количества молочной кислоты (лактата), кетокислот и других органических кислот.
Основными органами, участвующими в поддержании pH крови, являются легкие и почки.
- Легкие избавляют организм от кислот, за счет выдыхания CO2. По мере того как частота дыхания увеличивается или уменьшается, количество выдыхаемого CO 2 изменяется, что может изменить pH крови в считанные секунды или минуты.
- Почки выводят кислоты с мочой и влияют на концентрацию бикарбонатов (бикарбонатов, HCO 3 -) в крови; они щелочные по природе. Изменения pH из-за увеличения или уменьшения концентрации HCO 3 – происходят намного медленнее, чем в случае CO 2, на это уходят часы или дни.
Оба процесса работают постоянно, и очень тщательно контролируют pH крови здоровых людей. Также помогают регулировать концентрацию кислот и оснований буферные системы, предотвращающие большие колебания pH. Основные буферы крови включают гемоглобин (в красных кровяных тельцах), белки плазмы, бикарбонаты и фосфаты.
Абсолютное количество кислот или оснований менее важно для изменения pH крови, чем баланс между ними.
Ацидоз может быть вызван повышенным образованием кислоты в организме, приемом веществ, которые могут метаболизироваться до кислот, снижением экскреции кислоты или, наоборот, увеличением потерь оснований.
Алкалоз может возникать в результате изменений концентрации электролитов, таких как продолжительная рвота или сильное обезвоживание во время приема или потребления щелочей и гипервентиляции (с повышенным выделением кислот в форме CO 2). Любое заболевание или состояние, которое влияет на легкие, почки, метаболизм или дыхание, может вызывать ацидоз или алкалоз.
Нарушения кислотно-щелочного баланса делятся на две основные группы:
- Нарушения, влияющие на дыхание и приводящие к изменению уровня CO2, называются респираторным ацидозом (низкий pH) и респираторным алкалозом (высоким pH). Респираторные нарушения кислотно-щелочного баланса обычно вызваны заболеваниями легких или состояниями, влияющими на нормальное дыхание.
- Расстройства, которые изменяют концентрацию HCO3 – называются метаболическим ацидозом (низкий рН) и метаболический алкалоз (высокий рН). Метаболические нарушения кислотно-щелочного баланса могут быть вызваны заболеванием почек, изменением уровня электролитов, сильной рвотой или диареей, приемом некоторых лекарств или ядов, а также заболеваниями, влияющими на нормальный обмен веществ (например, сахарный диабет).
Симптомы
Ацидоз может не сопровождаться какими-либо симптомами или может сопровождаться неспецифическими симптомами, такими как усталость, тошнота и рвота. Острый ацидоз также может вызывать учащение и глубину дыхания, спутанность сознания и головную боль, а также может привести к потере сознания, коме и, в некоторых случаях, к смерти.
Симптомы алкалоза часто связаны с потерей калия (K +) и могут включать раздражительность, слабость и судороги.
Распространенные причины кислотно-щелочного дисбаланса
Респираторный ацидоз. Снижение экскреции CO2:
- снижение дыхания (гиповентиляция) из-за лекарств или нарушений центральной нервной системы;
- респираторный дистресс из-за травмы или из-за наличия воздуха между легкими и грудной стенкой (пневмоторакс);
- заболевания дыхательных мышц или нервов (миастения, ботулизм, боковой амиотрофический склероз (БАС), синдром Гийена-Барре);
- обструкция дыхательных путей (пища или инородное тело);
- заболевание легких.
Респираторный алкалоз. Повышенная экскреция CO2:
- учащенное дыхание (гипервентиляция) при страхе, боли, шоке;
- лекарства (например, при передозировке аспирином);
- пневмония, застой в легких или тромбоэмболия легочной артерии;
- перегрузка, лихорадка;
- опухоли, травмы или инфекции (менингит, энцефалит) центральной нервной системы;
- печеночная недостаточность.
Метаболический ацидоз. Снижение HCO 3 из-за потери HCO 3 или увеличения производства кислоты:
- алкогольный кетоацидоз;
- диабетический кетоацидоз;
- почечная недостаточность;
- лактоацидоз (обычно при недостатке кислорода в тканях);
- отравление – передозировка салицилатами (аспирин), метанолом, этиленгликолем;
- потеря бикарбонатов пищеварительным трактом, например, при длительной диарее;
- неспособность почек производить кислую мочу.
Метаболический алкалоз. Повышенный уровень HCO 3 – из-за потери кислоты или приема бикарбоната:
- диуретики;
- длительная рвота;
- сильное обезвоживание;
- прием бикарбонатов, прием щелочных веществ внутрь.
Диагностика
Цель обследования – выяснить, есть ли у обследуемого кислотно-щелочной дисбаланс, определить, насколько сложно это расстройство, чтобы помочь диагностировать основное заболевание или состояние (например, диабетический кетоацидоз, отравление и т. д.).
Вызвавшее расстройство. Обследование также проводится при наблюдении за тяжелобольными пациентами, а также в условиях, которые, как мы знаем, влияют на кислотно-щелочной баланс, например, при хронических заболеваниях легких или почек.
Основные тесты, используемые для выявления, оценки и мониторинга кислотно-щелочного дисбаланса:
- газы крови;
- анализ на электролиты.
Газы крови – это группа тестов, выполняемых вместе, обычно на основе образца артериальной крови (кровь, полученная из артерии, а не вены). Они отображают pH, pO2 (количество кислорода) и pCO2 (количество углекислого газа) в крови. По этим результатам можно рассчитать концентрацию бикарбонатов (HCO 3 -).
Для большинства случаев кислотно-щелочного дисбаланса значения HCO3 – и I pCO2 выходят за пределы допустимого диапазона. Это связано с тем, что организм пытается поддерживать уровень pH крови близким к норме. Следовательно, если одно из этих веществ является аномально высоким или низким, концентрация другого изменится в том же направлении, чтобы вернуть pH крови к норме. Этот процесс называется компенсацией. В таблице ниже показаны ожидаемые значения для каждого из четырех основных кислотно-щелочных дисбалансов.
Значения наблюдаются при четырех основных нарушениях кислотно-щелочного баланса:
| Ошибка ABR | pH | HCO 3 – | pCO 2 | Компенсация деятельности организма |
| Метаболический ацидоз | <7,36 | Низкий | Низкий | Увеличение частоты дыхания (гипервентиляция) для снижения CO 2 |
| Метаболический алкалоз | > 7,44 | Высокая | Высокая | Медленное дыхание (гиповентиляция) для увеличения выведения CO 2. |
| Респираторный ацидоз | <7,36 | Высокая | Высокая | Почки задерживают HCO 3 – и увеличивают выведение кислоты. |
| Респираторный алкалоз | > 7,44 | Низкий | Низкий | Почки уменьшают всасывание HCO 3 – и выведение кислот |
Электролиты представляют собой четыре теста: Na + (натрий, натрий), K + (калий, калий), Cl – (хлориды) и бикарбонаты (HCO 3 -), которые обычно рассчитываются по pH и CO2. Содержание жидкости в организме, концентрация электролитов и кислотно-щелочной баланс взаимосвязаны; при кислотно-щелочном дисбалансе концентрация одного или нескольких электролитов обычно повышается или понижается.
У пациентов с метаболическим ацидозом так называемая анионная щель рассчитывается с использованием концентраций электролитов; помогает узнать, какие нарушения могут быть причиной нарушения кислотно-щелочного баланса. Например, увеличение анионной щели указывает на ацидоз, например, диабетический.
Пациенты с метаболическим алкалозом обычно имеют низкие уровни хлорида (Cl -) и калия (K +), что снова является ориентиром для выявления причины кислотно-щелочного дисбаланса. На основании этих результатов могут потребоваться дополнительные тесты для выявления заболевания или состояния, вызывающего ацидоз или алкалоз (например, глюкоза, лактат, кетоновые тела, осмоляльность, метанол, этиленгликоль, токсикологические тесты на передозировку некоторыми лекарствами, индикаторы сепсиса и т. д.).
Бывает, что у пациента одновременно наблюдается более одного кислотно-щелочного дисбаланса. Примерами являются прием аспирина (который может вызвать как респираторный алкалоз, так и метаболический ацидоз) или люди с заболеваниями легких, принимающие диуретики (респираторный ацидоз плюс метаболический алкалоз). Используя номограммы для расчета ожидаемой степени компенсации, можно определить, присутствует ли смешанный кислотно-щелочной дисбаланс.
Лечение
Лечение ацидоза и алкалоза включает выявление и устранение причины, вызвавшей расстройство. Пациенту необходимо оказать необходимую поддержку. В большинстве случаев повышенный или пониженный pH не лечится напрямую. Однако в некоторых случаях врачи могут ввести в вену HCO3 – людям с опасно низким pH крови.
Источники: Статья «Ацидоз и алкалоз» на американском сайте Lab Tests Online; БЕРТИС, Калифорния, ЭШВУД, Эр., Брунс, Делавэр, (ред.), Учебник Тиц по клинической химии и молекулярной диагностике. 4-е издание Луи: Эльзевье-Сондерс, 2006; JABOR, A. et al .: Внутренняя среда. Praha: Grada Pulbishing, 2008; Kasper, DL., Braunwald, E., Fauci, AS., Hauser, SL, Longo, DL., Jameson, JL. (ред.) «Принципы внутренней медицины» Харрисона, 16-е издание, 2005.
- Авторы
- Файлы
- Литература
Моррисон В.В.
1
Чеснокова Н.П.
1
Бизенкова М.Н.
1
1 ГБОУ ВПО «Саратовский государственный медицинский университет им. В.И. Разумовского» Минздрава России
1. Агапов Ю.Я. Кислотно-щелочной баланс. – М.,1968. 184 с.
2. Войнов В.А. Атлас по патофизиологии. – М., 2004. – 218 с.
3. Гусев Г.П. Роль почки в регуляции кислотно-щелочного баланса // Физиология почки: Руководство по физиологии. – Л., 1972. – С. 142–168.
4. Жалко-Титаренко В.Ф. Водно-электролитный обмен и кислотно-основное состояние в норме и патологии. – Киев, 1989.
5. Комаров Ф.И., Коровкин Б.Ф., Меньшиков В.В. Биохимические исследования в клинике. – Л., 1981. – С. 249–273.
6. Костюченко С.С. Кислотно-щелочной баланс в интенсивной терапии. – Минск, 2009. – 268 с.
7. Лосев Н.И., Войнов В.А. Физико-химический гомеостаз организма // Гомеостаз / Под ред. П.Д. Горизонтова. – М., 1981. – С. 186–240.
8. Малышев В.Д. Кислотно-основное состояние и водно-электролитный баланс в интенсивной терапии: Учебное пособие. – М.: ОАО «Издательство «Медицина», 2005. – 228 с.
9. Неговский В.А., Гурвич А.М., Золотокрылина Е.С. Кислотно-основное равновесие // Постреанимационная болезнь. – М., 1987. – С. 70–83.
10. Рут Г. Кислотно-щелочное состояние и электролитный баланс. – М., 1978. – 118 с.
11. Тавс Г. Газы крови и кислотно-щелочное равновесие // Физиология человека. Т.3 / Под ред. Р. Шмидта и Г. Тавса. – М., 1986. – С. 241–268.
12. Хейтц У., Горн М. Водно-электролитный и кислотно-основный баланс: краткое руководство. – М.: БИНОМ. Лаборатория знаний, 2009. – 359 с.
13. Хруска К. Патофизиология кислотно-основного обмена // Почки и гомеостаз в норме и патологии. – М., 1987. – С. 170–216.
Все нарушения кислотно-основного гомеостаза по направлению сдвига концентрации водородных ионов делят на ацидозы и алкалозы.
Ацидозом называется такое нарушение кислотно-основного баланса, при котором в крови появляется абсолютный или относительный избыток кислот и повышается концентрация водородных ионов.
Алкалоз характеризуется сдвигом соотношения кислот и оснований, при котором происходит увеличение абсолютного или относительного количества оснований и понижается концентрация водородных ионов.
По степени компенсации все ацидозы и алкалозы подразделяются на компенсированные и некомпенсированные. Компенсированные ацидоз и алкалоз – это такие состояния, когда изменяются абсолютные количества Н2СО3 и NаНСО3, но отношение Н2СО3:NаНСО3 остается в пределах обычных колебаний (около 1:20). При сохранении этого отношения рН крови существенно не изменяется, т.е. остается в пределах 7,35–7,45. Соответственно некомпенсированными ацидозами и алкалозами называют такие состояния, когда изменяется не только общее количество, но и соотношение компонентов бикарбонатного буфера, вследствие чего наступает сдвиг рН за пределы нормальных границ.
По механизмам развития ацидозы и алкалозы подразделяются на газовые (дыхательные, респираторные) и негазовые.
Классификация нарушений кислотно-основного состояния:
1. Газовый (дыхательный) ацидоз.
2. Негазовый ацидоз:
а) метаболический;
б) выделительный;
в) экзогенный;
г) комбинированные формы (сочетание различных видов негазовых ацидозов).
3. Смешанный ацидоз (газовый + негазовый).
4. Газовый (дыхательный) алкалоз.
5. Негазовый алкалоз:
а) выделительный;
б) экзогенный.
6. Смешанные формы ацидозов и алкалозов (респираторный алкалоз компенсированный метаболическим ацидозом; негазовый алкалоз, компенсированный респираторным ацидозом).
Негазовый ацидоз – самая частая и тяжелая форма нарушения кислотно-основного состояния, с которой приходится встречаться врачам всех специальностей.
Причины негазового ацидоза разнообразны. Он наблюдается при дополнительном поступлении в организм ионов водорода или при потере бикарбоната из внеклеточной жидкости. Наиболее быстро и тяжело он развивается при гипоксии любого происхождения. Избыточное образование недоокисленных продуктов обмена (молочная, пировиноградная кислоты, ацетоновые тела и др.) наблюдается при сахарном диабете, голодании, тяжелой физической работе, обширном воспалении, при тяжелых поражениях печени.
Лактоацидоз может быть у пациентов с лейкозами, лимфомами, лимфогранулематозом и другими злокачественными новообразованиями.
Лекарственные средства, ингибирующие функции митохондрий, также могут вызывать угрожающий жизни лактат ацидоз. К ним относятся бигуаниды, использующиеся для лечения сахарного диабета и противовирусные нуклеозидные аналоги, используемые для лечения ВИЧ инфекции.
Лактоацидоз может быть обусловлен накоплением в крови D-лактата (продукта метаболизма бактерий кишечника) при синдроме слепой петли и кишечной непроходимости. В этих случаях неабсорбированные углеводы попадают в толстую кишку, где он превращаются в D-молочную кислоту при чрезмерно быстром росте грам-положительных анаэробов.
Лактоацидоз также может быть связан с наследственными нарушениями метаболизма: дефицитом глюкозо-6-фосфатазы или другими врожденными заболеваниями с дефектом глюконеогенеза или окисления пирувата.
Источником избыточных ионов водорода могут служить попадающие в организм уксусная кислота, салицилаты, хлористый аммоний, а также интоксикации этиленгликолем, метанолом. Экзогенный ацидоз может возникнуть также при длительном употреблении кислой пищи.
Выделительный ацидоз развивается при различных заболеваниях почек, которые сопровождаются нарушениями механизмов секреции в канальцах водородных ионов, аммиака, реабсорбции натрия и бикарбоната. Потере бикарбоната с мочой и развитию негазового ацидоза способствуют также введение солей калия, длительное лечение диакарбом. Определенную роль в развитии ацидоза играет гастроинтестинальная потеря бикарбоната (длительная диарея, свищи кишечника, желчных и панкреатических протоков).
Избыточное накопление водородных ионов в этих случаях компенсируется связыванием их буферными системами и концентрация бикарбонатов при этом уменьшается (ВЕ меньше – 2 ммоль/л, SB, ВВ и АВ – ниже нормы). Наступивший в буферных системах сдвиг восстанавливается путем усиленного выведения углекислого газа за счет гипервентиляции легких.
Кислые эквиваленты усиленно выделяются также через почки, основания активно реабсорбируются в почках. Часть кислот нейтрализуются в почках за счет усиленного образования аммиака. В моче вследствие этого происходит повышение содержания кислот и их аммонийных солей. Увеличение образования аммиака в почках сопровождается торможением образования мочевины в печени.
Механизмы развития негазового ацидоза несколько отличаются при различных видах патологии. Так, при гипоксии происходит нарушение обмена углеводов, преобладает анаэробный гликолиз, вследствие чего накапливаются избыточные количества молочной кислоты в крови – развивается лактат-ацидоз.
При сахарном диабете ацидоз является результатом накопления кетоновых тел (кетоацидоз) вследствие усиленного их образования при распаде высших жирных кислот. Избыточное образование кетокислот (β-оксимасляной и ацетоуксусной), по-видимому, зависит от двух факторов: 1) повышенного липолиза, увеличивающего поступление в кровь свободных жирных кислот; 2) преимущественного превращения свободных жирных кислот в печени в кетокислоты, а не триглицериды.
Голодание вызывает развитие ацидоза вследствие недостатка углеводов, что, в свою очередь, способствует мобилизации жира из депо. Увеличивается окисление жирных кислот в печени и, поскольку не хватает углеводов, происходит неполное окисление жирных кислот, накапливаются кетоновые тела.
Алкогольный кетоацидоз развивается в результате прямого ингибирующего действия этанола на глюконеогенез и прямого стимулирующего влияния на липолиз. Метаболический ацидоз при алкогольной интоксикации обусловлен не только увеличением продукции кетокислот, но и молочной кислоты.
При гломерулонефрите происходит ограничение выведения органических кислот с мочой в свободном виде и в виде аммонийных солей. Компенсация сдвигов в этих случаях может осуществляться за счет мобилизации натрия и других катионов из костей. Состояние ацидоза тормозит активность щелочной фосфатазы костной ткани и вызывает мобилизацию кальция и фосфора из костей.
Негазовый ацидоз часто диагностируется у больных на поздних стадиях хронической почечной недостаточности. Он развивается в результате снижения общей экскреции кислот. Снижение суммарной экскреции кислот происходит в основном из-за уменьшения экскреции NН4+. При этом в крови наблюдаются очень низкие значения буферных оснований, падает концентрация в крови хлора.
Другим вариантом почечного ацидоза является канальцевый ацидоз.
Экзогенный ацидоз возникает при употреблении некоторых лекарственных препаратов и отравлениях. Его причины: переливание большого количества растворов с рН ниже 7,0; отравления салицилатами, хлоралгидратом, суррогатами алкоголя, этиленгликолем; длительное употребление кислых продуктов. Метанол и этиленгликоль превращаются в кислые метаболиты, метанол – в муравьиную кислоту, этиленгликоль – в глиоксиловую и щавелевую кислоты. Отравление метиловым спиртом и салицилатами активирует также продукцию молочной кислоты, способствуя развитию лактацидоза. Некоторые сахара, применяемые для парентерального питания (фруктоза), также могут вызвать лактацидоз.
При негазовом ацидозе могут развиваться различные патологические изменения в органах и системах. При умеренном снижении рН сосуды, как правило, расширяются, что приводит к снижению артериального и венозного давления, уменьшению венозного возврата крови к сердцу и, следовательно, падению ударного и минутного объемов сердца. Однако при выраженном ацидозе возможно и сужение периферических сосудов.
Неизбежным следствием негазового ацидоза являются нарушения водно-электролитного баланса. С мочой теряется больше, чем в норме натрия, калия, кальция. Понижается их общее количество в тканях организма. Развившаяся при негазовом ацидозе гиперкалиемия в сочетании с низким содержанием калия в мышечной ткани, с изменением чувствительности кардиомиоцитов к ионам кальция и катехоламинам может привести к нарушению нервно-мышечной возбудимости и проводимости, возникновению экстрасистолии, мерцанию желудочков сердца, параличу скелетной мускулатуры.
Кровоснабжение мозга в условиях негазового ацидоза резко снижается за счет сужения просвета сосудов, питающих мозг, и падения системного давления из-за снижения деятельности миокарда.
При негазовом ацидозе возможно развитие микроциркуляторных расстройств в результате усиления агрегации тромбоцитов и возникновения тромбозов.
Со стороны дыхательной системы имеет место гипервентиляция за счет увеличения глубины и частоты дыхания. При снижении рН менее 7,2 может развиваться дыхание Куссмауля.
Вследствие расстройств функции сердца и периферического кровообращения, вторично нарушаются функция печени, центральной нервной системы (от оглушения до сопора). Негазовый ацидоз закономерно сопровождается уменьшением объема выделяемой мочи. Это объясняется значительным снижением доставки крови к почкам из-за угнетения гемодинамики, сужения почечных сосудов. Возможное снижение артериального давления и падение деятельности миокарда также отрицательно сказываются на кровоснабжении почек.
Возможно развитие гастроэзофагита с рвотой в связи с экскрецией протонов через слизистые желудочно-кишечного тракта.
Газовый ацидоз – нередкая форма нарушения кислотно-основного состояния организма. Первичным механизмом сдвига равновесия в сторону избытка водородных ионов при нем является избыток в крови углекислоты. В связи с этим наиболее частыми причинами респираторного ацидоза являются:
1) все виды заболеваний дыхательного аппарата, при которых нарушается газообмен между альвеолами и кровью или внешним воздухом (хронические обструктивные заболевания легких, отек легких, пневмония, бронхиальная астма, эмфизема, интерстициальный фиброз, легочный саркоидоз, коллагенозы, гемо- и пневмоторакс и др.);
2) угнетение дыхательного центра морфиноподобными препаратами, при травмах, воспалении, отеке головного мозга, при передозировке барбитуратами и др.;
3) нарушение проходимости дыхательных путей (аспирация инородных тел, астматический статус и др.);
4) резкие нарушения кровообращения, при которых кровоток замедляется настолько, что образующийся углекислый газ не успевает удаляться из крови в легких;
5) дыхание воздухом или газовыми смесями с высокой концентрацией углекислого газа;
6) парезы и параличи дыхательной мускулатуры различного генеза (полиомиелит, нейропатии, миастения, лечение миорелаксантами и др.).
Все эти патологические состояния ведут к гиповентиляции легких и гиперкапнии. Это, в свою очередь, приводит к уменьшению сродства гемоглобина к кислороду, а также уменьшению поступления кислорода в ткани, т.е. к гипоксии. Возникают условия, ведущие к усилению ацидоза за счет метаболических сдвигов вследствие недостаточного окисления продуктов межуточного обмена в клетках.
Этому процессу препятствуют буферные системы организма, в первую очередь, бикарбонатный буфер, емкость которого возрастает за счет накопления в крови углекислого газа, что ведет к увеличению концентрации бикарбонатов крови. Наблюдается сдвиг и в фосфатной буферной системе в сторону увеличения доли однозамещенных фосфатов.
Дыхательный механизм часто не может помочь в компенсации респираторного ацидоза, поскольку происхождение этой формы ацидоза связано с несостоятельностью функции легочной вентиляции.
Почки играют важную роль в поддержании нормального уровня рН при дыхательном ацидозе. В канальцах почек активнее секретируются ионы водорода; с мочой больше выделяется титруемых кислот и аммония хлорида, с другой стороны – усиливается реабсорбция бикарбоната и натрия.
При некомпенсированном дыхательном ацидозе увеличение напряжения углекислого газа в крови приводит к снижению рН. Если дыхательный ацидоз компенсируется метаболическими сдвигами, то величины ВВ, SВ, АВ возрастают, возникает избыток оснований (величина ВЕ более + 2 ммоль/л). Решающее значение имеет гемоглобиновый буфер эритроцитов, с помощью которого избыточная угольная кислота, давая начало повышенному образованию бикарбоната, пополняет им буферные основания плазмы.
Тяжесть нарушений в организме при газовом ацидозе зависит от степени избыточного накопления в крови углекислого газа и от присоединения метаболического ацидоза. При выраженном дыхательном ацидозе возникают расстройства, в первую очередь, со стороны сердечно-сосудистой системы. Вначале отмечаются усиление сердечной деятельности, учащение пульса, повышение минутного объема крови, подъем артериального давления. По мере углубления ацидоза происходит одновременное уменьшение активности α- и β-адренорецепторов сердца и сосудов, приводящее к угнетению сердечной деятельности и падению артериального давления. Появляются экстрасистолия и другие нарушения ритма вплоть до возникновения фибрилляции желудочков.
Сосуды головного мозга расширяются, усиливается образование ликвора, в результате чего возрастает внутричерепное давление.
Неблагоприятным следствием повышенного напряжения углекислого газа в крови являются спазм бронхиол, гиперсекреция слизи, что углубляет дыхательную недостаточность.
Спазм почечных сосудов снижает образование мочи из за ухудшения перфузии почечных клубочков.
Значительный избыток углекислого газа может вызвать коматозное или наркотическое состояние.
При газовом ацидозе содержание в крови ионов хлора умеренно снижается и имеется тенденция к гиперкалиемии.
Негазовый алкалоз – встречается реже ацидозов, но все-таки не является редкой формой патологии.
Первичным механизмом сдвига равновесия при негазовом алкалозе является потеря организмом нелетучих кислот или избыточное введение в организм оснований. В связи с этим причины, приводящие к развитию негазового алкалоза, немногочисленны. Это прием большого количества щелочных веществ (чаще бикарбоната натрия при изжоге, щелочных минеральных вод). Возникает негазовый алкалоз также при потере большого количества желудочного сока при частой и неукротимой рвоте, например при токсикозе беременных, при кишечной непроходимости, пищевых токсикоинфекциях; при желудочном свище, при многократном повторном отсасывании содержимого желудка. Нередко повторяющаяся рвота у детей бывает при пилоростенозе, при тяжелом коклюше. Причиной метаболического алкалоза может быть уменьшение экскреции и увеличение реабсорбции НСО3- в результате первичного или вторичного гиперальдостеронизма.
Негазовый алкалоз развивается при длительном лечении стероидными гормонами надпочечников. В этом случае возникает гипокалиемический алкалоз, вызванный обеднением плазмы крови и клеток калием вследствие его потери с мочой. Повышенная потеря хлора с мочой и гипохлоремический алкалоз бывают во время длительного лечения ртутными мочегонными и гипотиазидом.
Компенсация негазового алкалоза достигается благодаря угнетению дыхательного центра в результате снижения концентрации в организме водородных ионов. Однако такая компенсация не может быть длительной, поскольку гиповентиляция приводит к задержке в организме углекислого газа, развитию в результате этого гипервентиляции и нормализации напряжения углекислоты.
Компенсация также происходит за счет выведения и связывания избытка оснований. Этому в определенной степени способствует деятельность почек. При негазовом алкалозе с мочой может выделяться избыточное количество аниона бикарбоната, преимущественно в виде бикарбоната натрия. Образования кислых фосфатов и усиления аммониогенеза при этой форме патологии не происходит. Титруемых кислот в моче мало, она имеет щелочную реакцию.
Некоторую роль в компенсации негазового алкалоза играет белковый буфер, который в условиях накопления в организме оснований отдает в плазму ионы водорода, связывая катионы натрия. Часть избыточных анионов бикарбоната уходит в эритроциты и обменивается на ионы хлора.
Показателем некомпенсированного негазового алкалоза является повышение рН более 7,45, возрастание величин ВВ, АВ, SВ и, следовательно, возникновение избытка оснований (ВЕ более + 2,5 ммоль/л).
При некоторых состояниях наблюдается своеобразное течение этого патологического процесса из-за особенностей причин развития алкалоза. Так, при потере желудочного сока вследствие рвоты наблюдается потеря большого количества соляной кислоты, ионов хлора, хлористого натрия. При этом уменьшается выработка аммиака, увеличивается выведение бикарбоната и рН мочи может превышать 7,5.
Своеобразный вариант негазового алкалоза развивается при гипофункции паращитовидных желез. При недостатке паратгормона понижается выведение фосфорных солей с мочой, снижается содержание в крови кальция. Это приводит к повышению нервно-мышечной возбудимости, развитию судорог.
Поскольку альдостерон стимулирует секрецию калия и водорода, реабсорбцию натрия в дистальных почечных канальцах, избыточная выработка альдостерона может привести к потере ионов водорода и негазовому алкалозу. Влияние альдостерона на секрецию ионов водорода увеличивается при гипокалиемии. Действие альдостерона на секрецию ионов водорода и калия требует наличия натрия в канальцевой жидкости.
В связи с потерей через почки большого количества натрия при негазовом алкалозе наступает снижение осмотического давления во внеклеточной жидкости и чрезмерное выведение при этом воды, в результате чего происходит обезвоживание организма. В случае значительной потери калия может страдать функция миокарда, отмечаются нарушения со стороны центральной и периферической нервной системы.
Негазовый алкалоз гораздо легче предупредить, чем лечить. При оказании помощи больным с данным видом нарушения кислотно-щелочного баланса прежде всего стараются по возможности устранить действие вызывающей его причины. Далее возмещают дефицит ионов водорода, удаляют избыток бикарбоната, корригируют гипохлоремию и гипокалиемию, применяют антагонисты альдостерона.
Газовый алкалоз. Причинами газового алкалоза являются различные воздействия, повышающие объем легочной вентиляции и способствующие выделению углекислого газа из крови. Это наблюдается при дыхании разреженным воздухом на большой высоте. В этом случае появлению одышки и сопутствующей ей гипокапнии способствуют пониженное напряжение углекислого газа в атмосфере и возбуждение дыхательного центра вследствие кислородного голодания. Дыхательный алкалоз развивается также при одышке, возникающей при поражении мозга (травма, энцефалит, инсульт, опухоль и др.), при гипертермии, при избыточном приеме салицилатов. К респираторному алкалозу может привести психогенная гипервентиляция (истерия, беспокойство, интенсивный болевой синдром), сепсис, вызванный грамотрицательными бактериями, беременность вследствие влияния прогестерона на дыхательный центр, острая печеночная недостаточность в связи с накоплением аммиака, изменением соотношения глутаминовой кислоты, α-кетоглутарата в тканях мозга, в частности, дыхательного центра.
Необходимо отметить, что самопроизвольная одышка очень долго продолжаться не может, так как потеря большого количества углекислого газа ведет к падению возбудимости дыхательного центра и прекращению одышки. Этого не происходит при гипервентиляции при чрезмерном усилении искусственного дыхания с помощью аппаратов. Длительная искусственная вентиляция легких без контроля рСО2 крови может привести к тяжелому респираторному алкалозу, осложненному метаболическим ацидозом и глубоким угнетением дыхания.
Метаболическая компенсация дыхательного алкалоза сводится к уменьшению щелочных резервов крови (ВВ, SВ, АВ – ниже нормы, ВЕ смещается в сторону дефицита оснований) и накоплению водородных ионов. В этой компенсации основная роль принадлежит почкам, которые при снижении рСО2 уменьшают секрецию водородных ионов и реабсорбцию бикарбоната. При этом пониженное содержание угольной кислоты уравновешивается соответствующим снижением НСО3- в крови и соотношение компонентов бикарбонатного буфера снова приближается к 1:20. Уменьшение в плазме анионов НСО3- вызывает выход ионов хлора из эритроцитов и гиперхлоремию. Ионы водорода освобождаются из клеток в обмен на ионы калия, поэтому при газовом алкалозе всегда существует угроза развития гипокалиемии.
В процессе потери с мочой НСО3- вместе с ним в виде NаНСО3 из крови неизбежно теряется катион натрия. В условиях повышения рН крови образование иона аммония подавлено, преобразование основных фосфатов в кислые ослаблено, титруемых кислот в моче мало, рН ее высок.
Определенную роль в компенсации сдвига при респираторном алкалозе играет белковый буфер, который в этих условиях диссоциирует с освобождением в плазму ионов водорода.
При компенсированном и субкомпенсированном дыхательном алкалозе клиническая симптоматика практически отсутствует, возможно некоторое уменьшение частоты дыхания. Клиническая картина при декомпенсированном алкалозе обусловлена сочетанием гиперкапнии, гипокалиемии и гипокальциемии. Развиваются разнообразные изменения, в основном, со стороны сердечно-сосудистой системы. Наблюдается снижение тонуса сосудов, что влечет за собой уменьшение артериального и венозного давления. Происходят депонирование крови, уменьшение объема циркулирующей крови и снижение венозного возврата крови к сердцу, уменьшение ударного и минутного объема сердца. Вследствие сопутствующей гипокалиемии могут наблюдаться нарушения сердечного ритма. Тяжелый алкалоз может сопровождаться нарушением сознания (апатия, ступор), дыханием типа Чейн-Стокса, гипотензией, брадикардией. Этот сиптомокомплекс называется «гипервентиляционный синдром».
Все это приводит к снижению тканевого кровотока, развитию гипоксии и метаболического ацидоза, который в этом случае должен рассматриваться как защитная реакция организма на респираторный алкалоз. Значительная гипокалиемия приводит к развитию адинамии, мышечной слабости, нарушениям сердечного ритма. Понижение в крови концентрации ионизированного кальция может приводить к судорожным явлениям. Развитие судорожного синдрома является своеобразным механизмом компенсации алкалоза, так как во время судорог образуется лактат.
В условиях падения рСО2 при гипервентиляции происходят сужение церебральных сосудов и уменьшение снабжения головного мозга кислородом.
Снижение в плазме концентрации осмотически активных солей натрия и калия при газовом алкалозе способствует потере с мочой большого количества жидкости и обезвоживанию.
В лечении респираторного алкалоза наибольшее значение имеют восстановление нормального давления, вдыхание карбогена, нормализация водно-электролитного баланса.
На практике, однако, простые формы нарушения кислотно-основного состояния, обусловленные действием одного фактора, встречаются реже, чем комбинированные, вызванные воздействием противоположных или однонаправленных факторов.
Показатели КОС организма и их величины у здоровых людей (по Siggaard-Andersen, 1979)
|
Показатель |
Основная характеристика |
Пределы нормальных показателей |
|
рН рСО2 рО2 АВ SB BB BE |
Величина активной реакции среды Напряжение углекислого газа – отражает концентрацию растворенного в плазме крови углекислого газа Напряжение кислорода – отражает концентрацию растворенного в плазме крови кислорода
Истинный бикарбонат крови – содержание
Стандартный бикарбонат – содержание ионов Сумма оснований всех буферных систем крови Избыток или дефицит оснований. Отрицательные значения ВЕ – относительный избыток некарбоновых кислот; положительные величины ВЕ – относительный дефицит некарбоновых кислот, потеря ионов водорода. |
Артериальная кровь – 7,35–7,45 Венозная кровь – 7,32–7,41 Артериальная и капиллярная кровь – 35–45 мм. рт. ст. (4,7–6,0 кПа) Артериальная кровь – 95–100 мм рт. ст. (12,6–13,3 кПа) Венозная кровь – 40–45 мм рт. ст. (5,3–6,0 кПа) 19–25 ммоль/л 20–27 ммоль/л 45–55 ммоль/л ± 2 ммоль/л |
Смешанные расстройства кислотно-основного состояния (по Winters,1966; Mitchell,1975)
|
Клиническое состояние |
рН |
Состояние компенсации |
Нераспираторный фактор (ВЕ, НСО3- |
Распираторный фактор (рСО2) |
|
Газовый ацидоз и негазовый алкалоз с гиперпротонозом |
Снижен |
Частичная первичная компенсация |
Повышен |
Повышен |
|
Газовый ацидоз и негазовый алкалоз с нормопротоно-зом |
Норма |
Полная первичная компенсация |
Повышен |
Повышен |
|
Газовый ацидоз и негазовый алкалоз с гипопротонозом |
Повышен |
Частичная первичная компенсация |
Повышен |
Повышен |
|
Газовый алкалоз и негазовый ацидоз с гиперпротонозом |
Снижен |
То же |
Снижен |
Снижен |
|
Газовый алкалоз и негазовый ацидоз с нормопротонозом |
норма |
Полная первичная компенсация |
Снижен |
Снижен |
|
Газовый алкалоз и негазовый ацидоз с гипопротонозом |
Повышен |
Частичная первичная компенсация |
Снижен |
Снижен |
|
Газовый ацидоз и негазовый ацидоз |
Снижен |
Декомпенсация |
Снижен |
Повышен |
|
Газовый алкалоз и негазовый алкалоз |
Повышен |
Декомпенсация |
Повышен |
Снижен |
111
Библиографическая ссылка
Моррисон В.В., Чеснокова Н.П., Бизенкова М.Н. КИСЛОТНО-ОСНОВНОЕ СОСТОЯНИЕ. ТИПОВЫЕ НАРУШЕНИЯ КИСЛОТНО-ОСНОВНОГО СОСТОЯНИЯ (ЛЕКЦИЯ 2) // Международный журнал прикладных и фундаментальных исследований. – 2015. – № 3-2.
– С. 273-278;
URL: https://applied-research.ru/ru/article/view?id=6530 (дата обращения: 22.03.2023).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)

Во избежание недопонимания между читателями и автором в начале поста хотелось бы дать ряд определений, которые мы собираемся использовать в дальнейшем.
Первое — это определения кислот и оснований. Здесь стоит сделать оговорку, что существует несколько теорий кислот и оснований, охватывающих все множество кислотно-основных взаимодействий и рассматривающих кислотные и основные свойства с различных позиций для различных условий, но — для буферных систем крови мы воспользуемся протолитической теорией Бренстеда-Лоури, с разъяснения которой мы и начнем свой рассказ.
Согласно Бренстеду-Лоури, кислоты представляют собой вещества, отдающие протон (ион водорода, или H+), а основания — вещества, присоединяющие протон. Сила кислоты зависит от ее способности отдать протон, а сила основания — от способности протон связать. Например, в растворе серной кислоты происходит следующее:
H2SO4 + H2O ⇄ H3О+ + HSO4–
Серная кислота (H2SO4) передает протон основанию (H2O), при этом образуется новая кислота (H3О+) и новое основание (HSO4–).
Подобным же образом может происходить реакция между соляной кислотой и аммиаком:
HCl + NH3 ⇄ NH4+ + Cl–
Соляная кислота (HCl) передает протон основанию (NH3), при этом образуется новая кислота (NH4+) и новое основание (Cl–).
Как было сказано выше, кислоты и основания бывают сильными и слабыми. Например, H2SO4 и HCl представляют собой сильные кислоты, так как они очень легко отдают протон в раствор; таким образом, сильные кислоты диссоциируют быстро и полностью. И наоборот, HSO4– и Cl– являются слабыми основаниями, так как слабо удерживают протон. В описанных выше реакциях равновесие сдвинуто в сторону образования более слабой кислоты (H3О+ и NH4+) и более слабого основания (HSO4– и Cl–) соответственно. Слабые кислоты (например, H2CO3) диссоциируют не полностью, а значит, концентрация протонов в растворах этих кислот будет ниже. Сильные основания (например, OH–) активно взаимодействуют с протонами в растворе, связывая их, а слабые основания (HCO3–) делают это менее активно.
Второе — единица рН — логарифмическая единица, выражающая концентрацию ионов водорода в растворе в эквивалентах на литр; обратно пропорциональна количеству протонов в растворе, т. е. при высоком содержании протонов рН понижается, при низком, соответственно, повышается.
Рассмотрим пример. Пусть есть 0,1 М (читается как децимолярный) раствор соляной кислоты. Попробуем рассчитать для него значение pH. Мы знаем, что pH = –lg[H+]. Соляная кислота является сильной и в водном растворе будет диссоциировать полностью. Значит, количество моль/л, или М, [H+] будет равно [HCl], то есть 0,1 М. Дальше нам нужно просто подставить это значение в формулу:
pH = –lg[0,1] ≈ – (–1) = 1
Таким образом, раствор 0,1 М соляной кислоты имеет pH, равную 1, что соответствует очень кислой среде.
Тут же стоит вспомнить, что нейтральный раствор характеризуется следующей особенностью — значение концентрации ионов водорода [H+] равно значению концентрации гидроксильных ионов [OH–] = 10–7 моль/л, или pH = pOH = 7,0.
Третье — кислотно-основное равновесие (КОР) — последнее и самое главное. Буферные системы — это системы, состоящие из компонентов (например, слабой кислота и ее соль с сильным основанием или кислотно-основная пара), поддерживающих определенную концентрацию протонов в растворе, то есть определенный pH среды. Кислотность буферных растворов почти не меняется при их разбавлении или при добавлении к ним некоторых количеств кислот или оснований. Так, буферная система способна обратимо связывать протон (ион водорода). При связывании ионов водорода в условиях их повышенного количества в растворе получается слабая кислота и соль сильной кислоты, например:
HCl + NaHCO3 ⇄ NaCl + H2CO3
И наоборот, при защелачивании среды происходит диссоциация вещества, выделяется слабое основание и вода:
H2CO3 + NaOH ⇄ NaHCO3 + H2O
В обоих случаях буферные системы препятствуют резкому изменению pH. С помощью буферных систем и осуществляется регуляция КОР в организме. Однако, при работе буферной системы один из ее компонентов расходуется и требует восстановления.
Рисунок 1 | Общий вид буферной системы
Значения рН в жидких средах организма в норме:
- рН артериальной крови равен 7,4 (изменения КОР, такие как ацидоз и алкалоз, рассматриваются относительно показателя рН в артериальной крови);
- рН венозной крови и тканевой жидкости — 7,35;
- рН внутриклеточной жидкости варьируется от 6,0 до 7,4 в зависимости от клеточного компартмента;
- рН мочи может меняться в пределах от 4,5 до 8,0 в зависимости от КОР в жидких средах организма, т. к. почки являются мощным регулятором КОР;
- наиболее низкий рН (0,8) в желудочном соке, который вырабатывают обкладочные клетки желудка.
Диапазон патологических значений рН, при которых человек может жить в течение нескольких часов, варьируется от 6,8 до 8,0.
Расстройства кислотно-основного равновесия (КОР) — это нарушения физико-химического гомеостаза. Кислотно-основное равновесие определяется соотношением ионов Н+ и ОН– . От их соотношения зависят активность ферментов, интенсивность метаболических процессов, функции ряда органов, чувствительность рецепторов к медиаторам, проницаемость клеточных мембран. Расстройства КОР сопровождают практически все заболевания. Поэтому так же, как и другие виды нарушений обмена веществ, расстройства КОР относятся к типовым патологическим процессам.
Выделяют 2 типа расстройств КОР: ацидозы и алкалозы.
Ацидоз
— это типовой патологический процесс, характеризующийся относительным или абсолютным понижением pH. Алкалоз — это типовой патологический процесс, характеризующийся относительным или абсолютным увеличением pH. Ацидозы и алкалозы могут быть компенсированными, субкомпенсированными и декомпенсированными.
Компенсированные формы связаны с сохранением жизнедеятельности клетки, в то время как некомпенсированные формы вызывают нарушения функции клетки. Показателем компенсации является величина рН артериальной крови. В норме, как уже было сказано выше, рН = 7,4 ± 0,05. Если величина рН снижается до 7,24 или увеличивается до 7,56 (колебания составляют ± 0,16), то можно говорить о развитии субкомпенсированных форм. В том случае, если эта величина превышает ± 0,16, можно говорить о развитии декомпенсированных форм ацидоза или алкалоза. По происхождению ацидозы и алкалозы бывают газовые (дыхательные) и негазовые (метаболические), которые в свою очередь делятся на подтипы. Наряду с газовыми и негазовыми формами ацидозов и алкалозов встречаются смешанные формы. Кроме того, ацидозы и алкалозы могут быть острыми и хроническими.
Существует три основные системы, регулирующие содержание протонов и препятствующих возникновению ацидоза и алкалоза:
1) Буферные системы организма — моментально регулируют содержание протонов в растворе путем их связывания, но они не способны вывести избыток протонов из организма. Работа буферных систем поддерживает рН крови в пределах 7,35–7,45, а сдвиг рН более чем на 0,4 в любую сторону ведет к гибели. В жидких средах организма существует несколько буферных систем:
— Бикарбонатная буферная система [H2CO3 / HCO3–] является основным буфером крови (до 53 % емкости от всех буферных систем);
— Гемоглобиновый буфер [HHb / Hb–] — до 35 % буферной емкости от всех буферных систем, является внутриклеточным буфером;
— Белковый буфер [HPr / Pr–] — до 7 % буферной емкости от всех буферных систем;
— Фосфатный буфер [H2PO4– / HPO42–] — до 5 % буферной емкости от всех буферных систем; действует преимущественно в костной ткани, моче и внутриклеточной жидкости;
— Аммонийный буфер [NH3 / NH4+] — действует преимущественно в моче.
2) Дыхательная система — регулирует КОР путем выведения избытка СО2, а следовательно и H2CO3, из внеклеточной жидкости.
3) Выделительная система — почки устраняют изменения КОР путем выведения избытка кислот или оснований с мочой; эта система работает гораздо медленнее, чем предыдущие, однако значительно эффективнее.
В первую очередь рассмотрим наиболее мощную систему из выше перечисленных, берущую на себя основную роль в регуляции КОР — бикарбонатную.
Бикарбонатная буферная система
состоит из водного раствора, содержащего слабую угольную кислоту (H2CO3) и слабое основание — бикарбонат-ион (HCO3–), который во внеклеточной жидкости чаще всего находится в виде натриевой соли (NaHCO3). Вначале стоит разобрать такое понятие, как диапазон буферного действия — диапазон pH, в котором будет эффективен данный буфер. Характеризуется величиной pK.
Для бикарбонатного буфера pK будет равно 6,1 ± 1 — это далеко от среднего значения pH в организме, поэтому мощность бикарбонатного буфера не слишком велика. Тем не менее, бикарбонатный буфер является наиболее эффективной буферной системой. Во-первых, концентрация бикарбоната во внеклеточной жидкости довольно высока, во-вторых, оба компонента буферной пары легко контролируются дыхательной (CO2) и мочевыделительной (HCO3–) системами.
Тонкий баланс pH возможен в основном только благодаря способности легких и почек изменять соотношение H2CO3 / NaHCO3 (CO2 / HCO3–). Бикарбонатный буфер является самым чувствительным и связывает до 40 % «лишних» ионов водорода. Он поддерживает pH=7,4. В связи с вышеперечисленными фактами бикарбонатный буфер является индикатором нарушения КОР и определение компонентов этого буфера — основа диагностики нарушения КОР.
Рисунок 2 | Схема работы бикарбонатной буферной системы
При добавлении сильной кислоты в буферный раствор протоны, образовавшиеся при ее диссоциации, нейтрализуются путем взаимодействия с ионом бикарбоната, в результате формируется угольная кислота, которая разлагается на воду и углекислый газ под воздействием фермента карбоангидразы. Избыток углекислого газа, стимулирует барорецепторы в области бифуркации аорты и каротидного синуса, усиливает вентиляцию легких и таким образом выводится из организма. В норме отношение HCO3– / H2CO3 = 20/1. При этом, как уже упоминалось, работа этой системы неразрывно связана с легкими. Рассмотрим реакцию подробней. При поступлении в кровь кислоты более сильной, чем угольная, происходит реакция обмена и образуется новая соль и угольная кислота. В результате благодаря связыванию введенной в систему кислоты концентрация ионов водорода значительно понижается. (А — анион)
NaHCO3 + НА ⇄ H2CO3 + NaА
Обратная реакция происходит при добавлении к раствору сильного основания: гидроксид-ион взаимодействует с угольной кислотой с выделением иона бикарбоната, в результате чего концентрация угольной кислоты и, как следствие, углекислого газа в растворе снижается, что тормозит дыхательный центр, снижает вентиляцию легких и задерживает углекислый газ в организме. При этом повышается количество бикарбонат-ионов в плазме крови, что впоследствии компенсируется почками путем выделения их избытка с мочой. Рассмотрим реакцию подробней. При поступлении оснований они реагируют с угольной кислотой в результате чего образуются соль угольной кислоты. (К — катион)
H2CO3 + КОН ⇄ КHCO3 + Н2О
Содержание компонентов карбонатной буферной системы точно регулируется почками, контролирующими выделение и реабсорбцию бикарбонатов, а также дыхательной системой, регулирующей выделение углекислого газа с дыханием.
Фосфатная буферная система состоит из водного раствора H2PO4– и HPO42–, преимущественно в форме натриевой соли; имеет небольшое значение для регуляции КОР во внеклеточной жидкости, однако играет основную роль в регуляции его в просветах почечных канальцев (обеспечивает выведение ионов водорода с мочой) и во внутриклеточной среде. Если добавить в этот раствор сильную кислоту, то протоны, образованные при ее диссоциации, будут связываться с HPO42–, преобразуясь в H2PO4–. При добавлении сильного основания гидроксид-анион будет реагировать с H2PO4–, образуя HPO42– и воду. Таким образом, изменения рН в обоих случаях будут незначительными. D В норме соотношение NaH2PО4/Na2HPO4 = 1/4, а в моче NaH2PО4/Na2HPO4 = 25/1.
Рисунок 3 | Схема работы фосфатной буферной системы
Фосфатная буферная система играет важную роль в регуляции КОР в просвете почечных канальцев в связи с тем, что концентрация фосфатов в канальцах растет. Кроме того рН мочи ниже рН других жидкостей организма и близок к значению константы диссоциации фосфатного буфера (pH = 6,8 = pK для фосфатного буфера), что позволяет ему работать на максимальных мощностях. По тем же причинам фосфатный буфер имеет большое значение в регуляции КОР во внутриклеточной жидкости.
Рассмотрим устройство фосфатной буферной системы подробней. Емкость фосфатной системы составляет около 1–2 % от всей буферной емкости крови и до 50 % буферной емкости мочи. Она образована дигидрофосфатом (NaH2PO4) и гидрофосфатом (Na2HPO4) натрия. Первое соединение (NaH2PO4) слабо диссоциирует и ведет себя как слабая кислота, второе (Na2HPO4) обладает щелочными свойствами. В норме отношение HРO42– к H2РO4 — равно 4 : 1.
При взаимодействии кислот (ионов водорода) с двузамещенным фосфатом натрия (Na2HPO4) натрий вытесняется, образуется натриевая соль дигидрофосфата (H2PO4–). В результате благодаря связыванию введенной в систему кислоты концентрация ионов водорода значительно понижается. (А — анион)
HРO42– + НА ⇄ H2PO4–+ А–
При поступлении оснований избыток ОН– групп нейтрализуется имеющимися в среде Н+, а расход ионов Н+ восполняется повышением диссоциации NaH2PO4 (К — катион)
H2PO4– + КОН ⇄ К+ + HРO42– + Н2О
Основное значение фосфатный буфер имеет для регуляции pH интерстициальной жидкости и моче. Как уже было отмечено выше в моче его роль состоит в сбережении бикарбоната натрия за счет дополнительного иона водорода (по сравнению с NaHCO3) в составе выводимого NaH2PO4.
Na2HPO4 + H2CO3 ⇄ NaH2PO4 + NaHCO3
Кислотно-основная реакция мочи зависит только от содержания дигидрофосфата, т. к. бикарбонат натрия в почечных канальцах реабсорбируется.
Белковая буферная система
играет основную роль в регуляции КОР внутри клетки в связи с их богатым содержанием во внутриклеточной жидкости.
Несмотря на разницу между значениями рН внутри клетки и вне ее, колебания внутриклеточного КОР находится в зависимости от внеклеточного. Компоненты бикарбонатной буферной системы медленно диффундируют через клеточную мембрану. Соответственно работа внутриклеточных буферных систем может оказывать посильную помощь в регуляции внеклеточного КОР, однако занимает этот процесс значительно большее время. Около 60–70 % буферной емкости всего организма приходится на белковые внутриклеточные системы, однако в связи с низкой скоростью переноса компонентов буфера через мембраны, коррекция КОР за счёт них может значительно опаздывать.
Сама по себе белковая буферная система состоит как из белков внутриклеточных, так и внеклеточных. Белки и их главные структурные компоненты, аминокислоты, являются амфолитами и потому в зависимости от величины pH среды способны принимать или отдавать ион водорода. Таким образом, кислые группы (например, COOH) могут отдавать ион водорода, при повышении pH, а аминогруппы (например, NH2) могут принимать ион водорода при падении pH. Пределы действия белковых кислотно-основных буферных систем ограничиваются количеством групп, способных отдавать или связывать ионы водорода. Жидкости организма, на основе их локализации, можно разделить на внеклеточные и внутриклеточные жидкости.
Рисунок 4 | Схема работы белковой буферной системы
К внеклеточным жидкостям тканей относятся межклеточные жидкости. Разновидностью межклеточных жидкостей является плазма крови. Плазма крови содержит белки, которые могут составляют одну буферных систем крови. Межклеточная жидкость в тканях содержит волокна внеклеточного белка и растворенные аминокислоты. Все эти компоненты составляют буферную систему межклеточных жидкостей в тканях. Основным белковым буфером в случае крови является гемоглобиновый буфер.
Гемоглобиновый буфер
— мощный регулятор КОР; представлен в эритроцитах и плазме крови, с тем отличием, что проникновение компонентов бикарбонатного буфера через мембрану эритроцитов происходит значительно быстрее, чем у других клеток. Эта буферная система включает в себя восстановленный гемоглобин (HHb) и калиевую соль восстановленного гемоглобина (KHb). Так, буферные свойства данной системы обусловлены тем, что калиевая соль гемоглобина является солью слабой кислоты и может обменивать ион калия, К+ на ион водорода, H+, при этом образуется слабодиссоциирующая кислота. Вот так:
H+ + KHb ⇄ К+ + HHb
Гемоглобин осуществляет буферирование за счет имидазольных групп гистидиновых остатков и имеет pKa = 6,8. Величина pH крови остаётся постоянной благодаря тому, что гемоглобин способен связывать углекислый газ и ионы водорода, тут гемоглобин играет роль основания. В легких находится окисленная форма гемоглобина HHbO2, которая является более сильной кислотой (при этом кислотность HHbO2 в 70 раз выше, чем у HHb), чем угольная кислота (H2CO3), в результате чего подавляется диссоциация последней. HHbO2 отдает свои ионы Н+ в среду, предотвращая повышение рН. В целом если говорить о крови, то ее буферные системы более устойчивы к действию кислот, чем оснований.
Рисунок 5 | Схема работы гемоглобиновой буферной системы
Буферные системы тканей предотвращают возможные деструктивные нарушения, причиной которых может быть действие продуктов метаболизма клеток, к которым относятся органические кислоты, такие как молочная кислота и пировиноградная кислота. Поскольку между внутриклеточными и внеклеточными жидкостями осуществляется непрерывный обмен веществами, внутриклеточные буферные системы работают вместе с внеклеточным буферными системами в поддержании кислотно-основного равновесия в целом. Когда во внеклеточной жидкостях уменьшается pH, клетки перекачивают ионы водорода из внеклеточной жидкости в цитоплазму клеток. При этом внутриклеточные белковые буферные системы мгновенно компенсируют увеличение кислотности. И наоборот, когда во внеклеточной жидкости увеличивается pH, транспортные механизмы цитоплазматических мембран клеток перекачивают ионы водорода из внутриклеточных жидкостей во внеклеточную жидкость. При этом, для сохранения ионного равновесия, во внутриклеточную жидкость из внеклеточной жидкости перекачиваются ионы калия K+.
Поскольку в организме все буферные системы в том или ином соотношении представлены во всех жидкостных средах, они действуют сообща. Смысл изогидрического правила заключается в том, что изменение равновесия в одной буферной системе в растворе ведет за собой изменение и в других системах за счёт перераспределения между ними ионов водорода.
Дыхательная система — регулирует концентрацию СО2 во внеклеточной жидкости. При повышении вентиляции СО2 активно выводится из организма, что вызывает снижение концентрации углекислоты и приводит к снижению количества протонов в крови. Снижение вентиляции вызывает повышение количества СО2 в крови, и концентрация ионов водорода в крови растет.
В клинической практике удобно использовать показатель парциального давления углекислого газа — рСО2, в норме равный 40 мм рт.ст. При повышении интенсивности метаболических процессов или уменьшении вентиляции легких рСО2 растет, накапливается углекислота и соответственно ионы водорода, приводя к снижению рН — ацидозу. Замедление метаболических процессов или рост вентиляции вызывает снижение СО2 в крови, количества протонов и приводит к алкалозу, что проявляется повышением рН.
Уровень рН в жидких средах организма очень чувствителен к изменению вентиляции. Так, увеличение вентиляции в 2 раза от нормы приводит к повышению рН на 0,23 единиц, при этом снижение альвеолярной вентиляции на ¼ ниже нормы влечет за собой снижение уровня рН на 0,45 единиц. Таким образом, становится понятно значение дыхательной системы в регуляции КОР.
В свою очередь деятельность дыхательной системы зависит от концентрации протонов в крови, то есть изменение рН во внеклеточной жидкости ведёт за собой изменение вентиляции, что является ярким примером принципа отрицательной обратной связи в системе (при работе такой связи, усилия системы направлены на возвращение к исходному состоянию организма). Рост концентрации протонов и сопутствующее ему повышение рН вызывает компенсаторное увеличение вентиляции вследствие стимуляции дыхательного центра. Напротив, уменьшение количества ионов водорода и повышение рН тормозят дыхательный центр. Таким образом, довольно быстро регулируется содержание протонов в системе.
Дыхательная система как физиологический буфер действует медленнее, чем любой из химических буферов, однако ее буферная емкость в 2 раза выше всех вместе взятых буферов внеклеточной жидкости. У нее довольно низкий коэффициент эффективности обратной связи, поэтому коррекция значений рН осуществляется в очень малых пределах, тем не менее, это позволяет выиграть время для стабилизации КОР с помощью выделительной системы.
При нарушениях функций дыхательной системы также происходит изменение уровня ионов водорода и соответственно показателя рН. При нарушении процесса нормальной вентиляции легких (например, при эмфиземе легких), снижается способность выведения СО2, в результате чего развивается дыхательный ацидоз. В такой ситуации коррекция КОР полностью перекладывается на выделительную систему.
Выделительная система почек
— осуществляют регуляцию КОР путем выделения кислых и основных продуктов обмена с мочой. В целом, принцип работы системы заключается в следующем: бикарбонат-ионы попадают в просвет канальцев с первичной мочой путем фильтрации, ионы водорода секретируются эпителиоцитами в просвет канальцев, где они связываются ионами бикарбоната и реабсорбируются обратно в кровь в форме угольной кислоты. Таким образом, осуществляется восполнение компонентов бикарбонатного буфера. Если количество протонов во внутриканальцевой жидкости превышает количество бикарбонат-ионов (при ацидозе), их избыток выводится с мочой, закисляя ее, и наоборот, избыток оснований способствует их выведению (при алкалозе). Эти процессы происходят во всех отделах канальцевой системы, исключая тонкий отдел петли Генле, при этом 80–90 % реабсорбции бикарбонатов и секреции протонов приходится на проксимальный каналец. В различных сегментах эти процессы осуществляются разными механизмами. Кроме того, с мочой выводятся нелетучие кислоты (те, которые не могут выделяться через дыхательную систему), полученные в ходе метаболических процессов, что в свою очередь увеличивает количество протонов в моче. Немаловажным механизмом регуляции КОР почками является образование новых ионов бикарбоната, опять же при участии карбоангидразы.
При выделении в мочу избытка протонов лишь небольшая их часть выводится в свободном виде, остальные связываются с буферными системами в просвете канальцев, способствуя выработке недостающего количества бикарбонатов внутри клеток канальцев с последующей их реабсорбцией в кровь при ацидозе. Наибольшее значение имеют фосфатная и аммонийная системы, меньшую роль играют цитратная и уратная.
Аммонийная буферная система
состоит из аммиака (NH3) и иона аммония (NH4+). При увеличении количества ионов водорода во внеклеточной жидкости, стимулируется дезаминирование глутамина в почке под действием глутаминазы с образованием 2 молекул NH3 секретируемых в просвет канальца. Глутамин поступает с током крови из печени в эпителиоциты проксимальных канальцев, толстого восходящего отдела петли Генле и дистальных канальцев. В собирательных трубочках выделение иона аммония происходит с помощью другого механизма, при этом вновь синтезируется и реабсорбируется в кровь один бикарбонат-ион. Более подробнее ниже. Активация карбоангидразы, приводит к образованию H2CO3, который диссоциирует с образованием H+ и HCO3–. Как NH3 так и HCO3– служат для связывания ионов водорода. При этом HCO3– выделяется в кровь, где связывается с ионом водорода, а ион водорода образовавшийся в клетке почечных канальцев при диссоциации H2CO3 секретируется в просвет почечного канальца, где связывается NH3 с образованием NH4+. При уменьшении количества ионов водорода во внеклеточной жидкости наблюдается противоположный ответ почек. Во время хронического ацидоза аммонийная система берёт на себя основную роль в выведении кислых продуктов с мочой.
Рисунок 6 | Схема работы аммонийной буферной системы
В заключение, приведенная в данной статье информация далеко не полная и не включает в себя многие нюансы, однако, прочитав данную информацию, можно получить общее представление о регуляции кислотно-основного равновесия в организме.
- Гайтон А. К., Холл Д. Э. Медицинская физиология. – 2008.
- Нельсон Д. Л., Кокс М. М., Ленинджер А. Основы биохимии Ленинджера. – 2011.
- Моррисон Р., Бойд Р. Органическая химия. – Мир, 1974. – С. 301-322.
- Покровский В. М. и др. Физиология человека. – Открытое акционерное общество Издательство Медицина, 2007.
- Миллера М. Р. А. Р. СПб //Человек. – 2015.
- Костюченко С. С. Кислотно-щелочной баланс в интенсивной терапии //Минск: ОИТАР МОКБ, ГрГМУ. – 2009.
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Кислотно-щелочное равновесие является важным параметром, который поддерживается в крови человека в определенных пределах. Это необходимо для нормального функционирования различных систем организма, протекания биохимических реакций, оптимального функционирования ферментов.
Кислотами называются вещества, которые могут отдавать ионы водорода, а основаниями (щелочами) вещества, присоединяющие данные ионы. Кислотность и щелочность растворов оценивается по шкале рН от 0 (растворы сильных кислот) до 14 (растворы сильных щелочей). По шкале рН нейтральная кислотность равна 7.
Нормальная кислотность крови составляет 7,35 – 7,45 по шкале рН. Смещение данного показателя ниже 7,35 свидетельствует об ацидозе (смещении кислотно-щелочного баланса крови в сторону увеличения кислотности). При отклонении рН выше 7, 45 возникает алкалоз (избыток веществ со свойствами щелочей в крови).
В процессе обмена веществ в организме в больших количествах образуются продукты, которые способны вызывать изменение данного параметра. Главную роль в регуляции кислотно-щелочного равновесия принадлежит легким, почкам и буферным системам крови.
Во время дыхания через легкие осуществляется выделение углекислого газа, который образуется в процессе обмена веществ в организме. Углекислый газ при соединении с водой образует углекислоту, поэтому в случае его избытка в крови развивается ацидоз, а при недостаточной концентрации углекислого газа возникает алкалоз.
Почки выводят с мочой из организма избыток кислот и щелочей. При этом данные органы в определенных пределах могут регулировать количество выделяемых и всасываемых обратно кислот и оснований, за счет чего происходит регуляция уровня рН в крови.
Буферными системами крови называют растворы слабых кислот и щелочей, которые соединяясь с избыточными количествами кислот или оснований (в зависимости от наличия ацидоза или алкалоза) осуществляют их нейтрализацию, чем достигается выравнивание уровня рН.
Причиной ацидоза и алкалоза в большинстве случаев является тяжелое течение основного заболевания, при котором возникающие изменения рН крови превышают возможности механизмов регуляции данного параметра.
Синонимы русские
Нарушения кислотно-щелочного равновесия крови, нарушения кислотно-щелочного гомеостаза.
Синонимы английские
Acid-Base Disorders, Acid–base homeostasis.
Симптомы
Проявления ацидоза и алкалоза часто маскируются проявлениями основного заболевания, которое вызвало изменение кислотно-щелочного баланса крови.
При ацидозе могут быть следующие симптомы:
- тошнота, рвота
- учащение частоты дыхания
- головная боль
- нарушение сознания (вплоть до комы)
- падение артериального давления (при тяжелых формах ацидоза)
- нарушения ритма сердца.
Проявления алкалоза могут включать в себя:
- головные боли
- головокружение
- угнетение сознания (вплоть до комы)
- судороги в различных группах мышц
- нарушения сердечного ритма
Общая информация о заболевании
Кислотно-щелочное равновесие в крови является жизненно важным параметром, нормальные значения которого составляют 7,35 – 7,45 по шкале рН.
Отклонение рН ниже 7,35 свидетельствует об ацидозе. При смещении рН выше 7,45 возникает алкалоз.
В зависимости от причин развития ацидоз и алкалоз делятся на метаболический (обменный) и респираторный (дыхательный).
Респираторный ацидоз развивается в результате накопления в крови большого количества углекислого газа, который соединяясь с водой, образует углекислоту. Это вызывает повышение кислотности крови. Данное состояние может развиваться при нарушениях дыхания, которые вызывают снижение легочной вентиляции.
Это может быть следствием заболеваний легких (например, при бронхиальной астме), поражений нервной системы (например, при травмах головного мозга), заболеваниях, мышц и нервов, которые приводят к потере способности совершать эффективные дыхательные движения (например, при боковом амиотрофическом склерозе).
Противоположным состоянием является респираторный алкалоз, который возникает при избыточном выведении легкими углекислого газа из организма. В основе механизма развития данного вида алкалоза лежит увеличение ритма и глубины дыхания.
Такое нарушение дыхания может возникать при наличии патологии со стороны различных органов и систем (например, при травмах, опухолях головного мозга, заболеваниях легких, сердечно – сосудистой недостаточности).
Метаболический ацидоз может развиваться по следующим причинам:
- повышение продукции кислот в организме. Повышение продукции кислот в организме может наблюдаться при состояниях, сопровождающихся нарушениями процессов обмена веществ. Например, при сахарном диабете нарушается использование глюкозы клетками по причине недостатка гормона инсулина.
При этом организм начинает вырабатывать энергию не из глюкозы, а из жиров – альтернативный путь получения энергии. Расщепление жиров в печени сопровождается образованием больших количеств кетоновых кислот, что приводит к возникновению ацидоза.
- нарушение функционирования почек. Почки выполняют важную роль в регуляции кислотно-щелочного баланса в крови. При заболеваниях почек, приводящих к нарушению их функций, могут нарушаться процессы выделения кислот и всасывания веществ со щелочной реакцией, что может быть причиной ацидоза.
- потеря больших количеств щелочей с пищеварительными соками. Данное состояние может наблюдаться при выраженной диарее, проведении хирургических вмешательств на кишечнике.
- отравление ядами и токсическими веществами. Процессы расщепления данных веществ в организме могут протекать с образованием большого количества кислот, что может стать причиной ацидоза.
Основными причинами метаболического алкалоза являются следующие:
- потеря больших количеств кислого желудочного содержимого. Может наблюдаться при обильной рвоте, аспирации содержимого желудка с помощью специального зонда.
- применение мочегонных препаратов
- усиленное выведение ионов водорода почками. Такие процессы могут наблюдаться при избытке гормона надпочечников – альдостерона. Альдостерон участвует в регуляции водно-электролитного баланса в организме. Повышение его уровня может быть как при заболеваниях надпочечников, так и при патологии других органов (например, при сердечной недостаточности).
Таким образом, развитие ацидоза или алкалоза часто связано с протеканием патологических процессов, при которых возникающие изменения кислотно-щелочного равновесия превышают компенсационные возможности организма. При этом важную роль в лечении занимает нормализация состояния пациента по осн









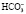 в истинной крови
в истинной крови
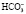 в пробе крови, приведенной к стандартным условиям (t = 37 °С, рСО2 – 40 мм рт. ст., содержание HbO2 – 100 %)
в пробе крови, приведенной к стандартным условиям (t = 37 °С, рСО2 – 40 мм рт. ст., содержание HbO2 – 100 %)